Begin april 2020 verschenen de eerste berichten in de media, dat het aantal kankerdiagnoses in Nederland ten gevolge van de coronacrisis terugliep. Deze constatering was gebaseerd op gegevens van het Pathologisch-Anatomisch Landelijk Geautomatiseerd Archief (PALGA). Omdat bij het overgrote deel van de patiënten met kanker de diagnose wordt gesteld met weefselonderzoek, was dit het eerste signaal dat de zorg voor oncologie patiënten onder druk stond als gevolg van de coronapandemie.
PALGA en het Integraal Kankercentrum Nederland (IKNL) concludeerden dat de daling in kankerdiagnoses mogelijk werd veroorzaakt door uitgestelde huisartsbezoeken, vertraagde diagnostiek en de opgeschorte bevolkingsonderzoeken1. In deze paragraaf beschrijven wij in detail de effecten van de COVID-19 crisis op de kwaliteit van de oncologische zorg in 2020, zoals deze jaarlijks wordt geëvalueerd in verschillende landelijke kwaliteitsregistraties. Het betreft zowel de kwaliteit van chirurgische behandelingen en bestralingsbehandelingen als de systemische behandeling met medicatie, zoals chemotherapie, immunotherapie en doelgerichte therapieën.
Oncologische chirurgie
Voor veel tumorsoorten, zoals borst-, hoofd-hals-, slokdarm-, maag-, alvleesklierkanker, darm-, lever- en gynaecologische kanker (en in mindere mate longkanker) bestaat de primaire behandeling uit een operatie waarbij de tumor wordt weggehaald. Deze chirurgische behandelingen variëren van operaties in dagbehandeling zoals die van de borst tot aan grote complexe oncologische operaties zoals bij alvleesklierkanker. In het laatste geval worden patiënten vijf tot tien dagen in het ziekenhuis opgenomen. Zij verblijven daarbij soms meerdere dagen op de Intensive Care (IC). De druk op de ziekenhuiscapaciteit (zowel op de operatie-, IC- als de verpleegafdelingen) ten gevolge van de COVID-19-pandemie kan impact hebben gehad op de zorg voor chirurgische oncologiepatiënten in 2020. Ook de uitgestelde diagnostiek kan consequenties hebben gehad voor de behandeling en prognose, bijvoorbeeld doordat patiënten bij klachten mogelijk later of niet naar hun huisarts zijn gegaan of door het uitstellen van het bevolkingsonderzoek. Daarbij kunnen tumoren mogelijk pas in een verder gevorderd stadium zijn ontdekt.
Aantal kankeroperaties gedaald
Over heel 2020 werden er in zeven kwaliteitsregistraties (waarin dertien tumorsoorten worden geregistreerd) circa 2000 complexe oncologische operaties minder gerapporteerd dan mag worden verwacht op basis van de referentieperiode (2018/2019). Dit is een daling van 11%. Daarnaast werden er in de periode van 11 maart tot 20 september 2020 (eerste golf en tussenperiode) 9.451 borstkankeroperaties uitgevoerd, terwijl er op basis van de referentieperiode 11.500 verwacht werden. Dit is een daling van 18%. In figuur 1 is te zien in welke perioden van 2020 de complexe oncologische ingrepen qua aantal achterbleven.
Figuur 1. Aantal complexe oncologische operaties in 2020, afgezet tegen het verwachte aantal o.b.v. 2018-2019
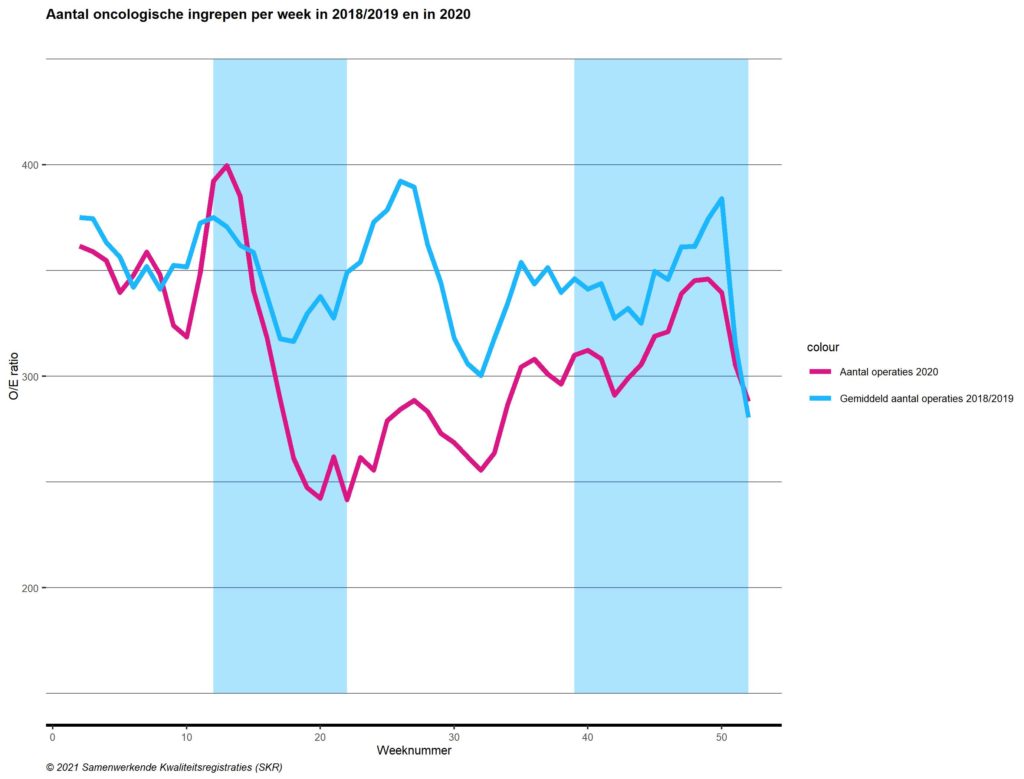
Achterstand
In figuur 1 is te zien dat tot de start van de eerste golf het aantal complexe oncologische operaties was zoals verwacht. In maart is een piek in het aantal operaties zichtbaar. Het zou kunnen dat men toen in de ziekenhuizen in het Midden en Noorden van het land anticipeerde op het feit dat de operatie- en IC-capaciteit op korte termijn onder druk zouden komen te staan. Daarna volgde een vermindering van het aantal complexe operaties, met 100 operaties per week (circa 30%). Het aantal operaties leek pas aan het eind van 2020 enigszins bij te trekken. In totaal zijn er in 2020 11% minder complexe oncologische operaties uitgevoerd dan verwacht werd op basis van de referentieperiode.
Regionale verschillen
Zoals in het hoofdstuk ‘De Pandemie In Beeld’ is beschreven, heeft de pandemie (en daarmee: de druk op de ziekenhuizen) zich niet gelijkelijk ontwikkeld over het land. Hierdoor was de druk op de kwaliteit van zorg in bepaalde periodes in sommige regio’s hoger dan in andere regio’s. In figuur 2 is het aantal complexe oncologische operaties weergegeven in de drie tijdsperiodes van 2020. We zien dat de complexe oncologische chirurgie tijdens de eerste golf in bijna alle ROAZ-regio’s (en in de tussenperiode in alle regio’s) was afgeschaald. Vooral de zuidelijke en oostelijke regio’s waren getroffen met tot 30% minder oncologische operaties. Vooral in Brabant, maar ook in de regio Gelderland en Leiden-Den Haag lijkt men in 2020 nauwelijks de mogelijkheid te hebben gehad om dit in te halen. Dit was anders dan in de meer noordelijke regio’s, waar in de tweede golf meer werd geopereerd dan verwacht.
Figuur 2. Regionale verschillen in curatieve oncologische chirurgie per ROAZ Regio in Nederland in 2020, afgezet tegen het verwachte aantal o.b.v. 2018-2019
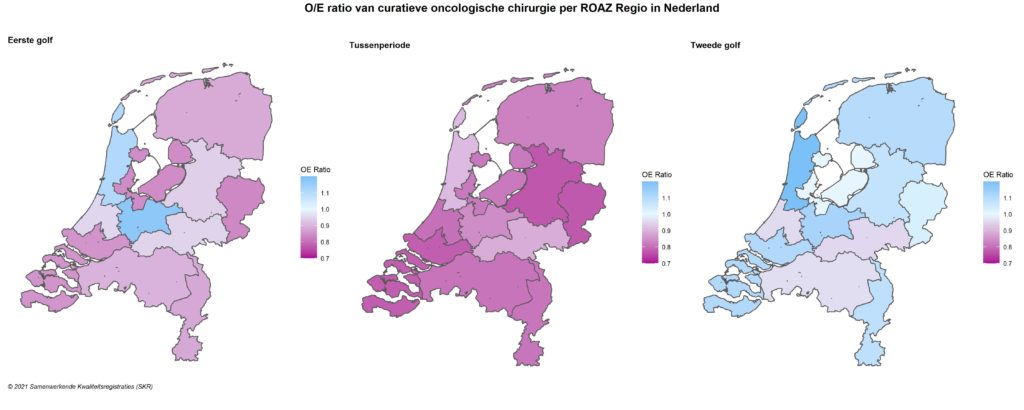
Verschillen tussen complexe ingrepen
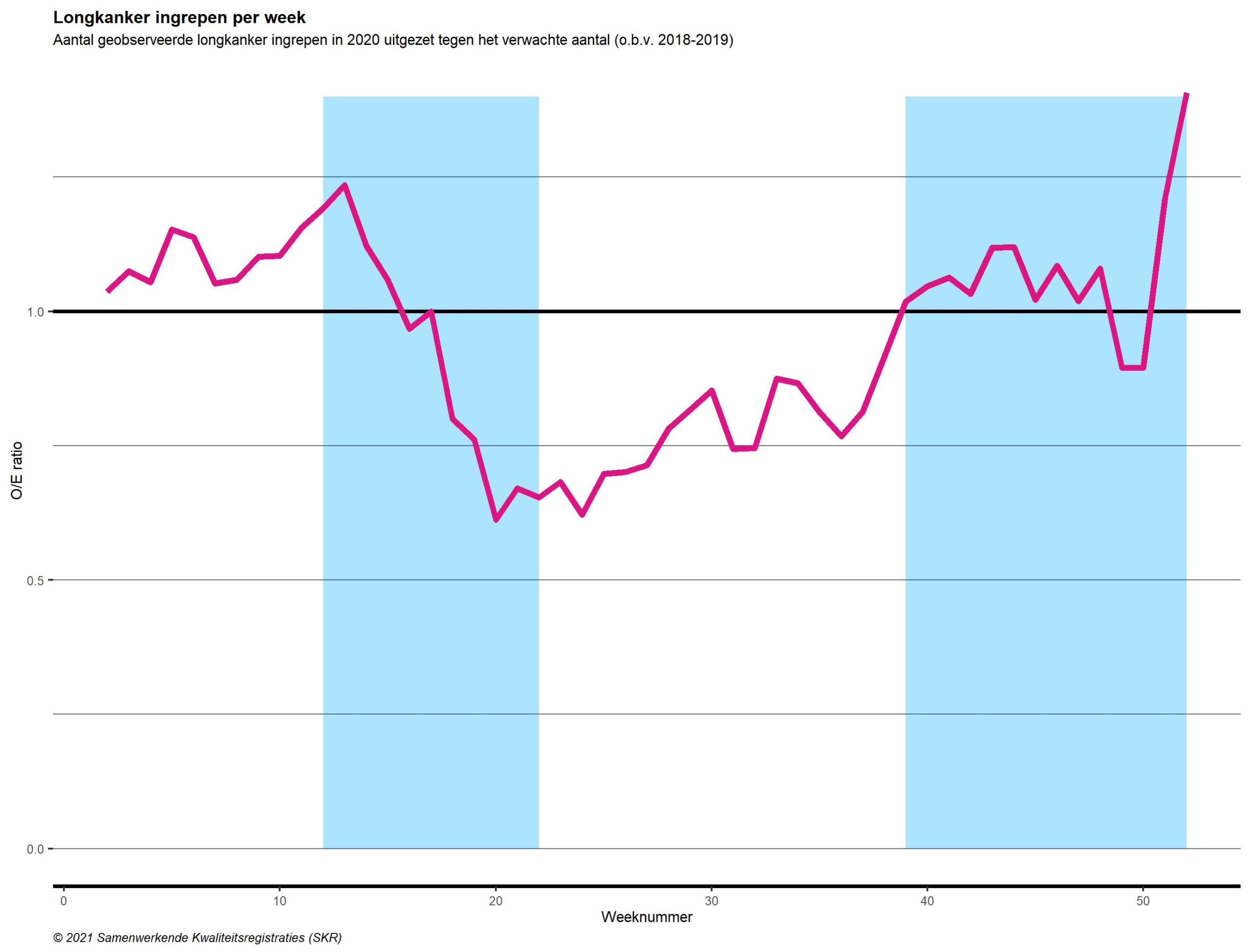
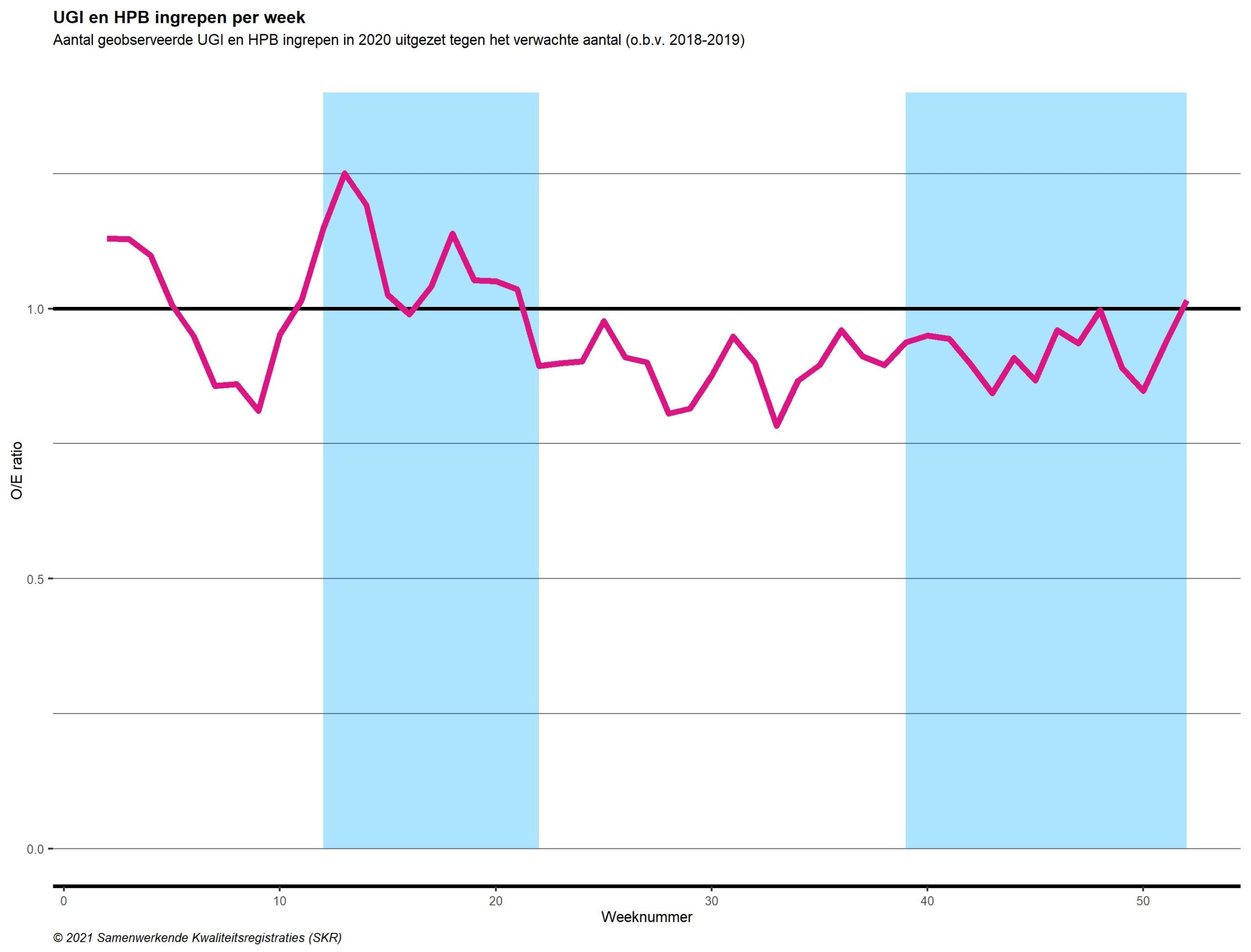
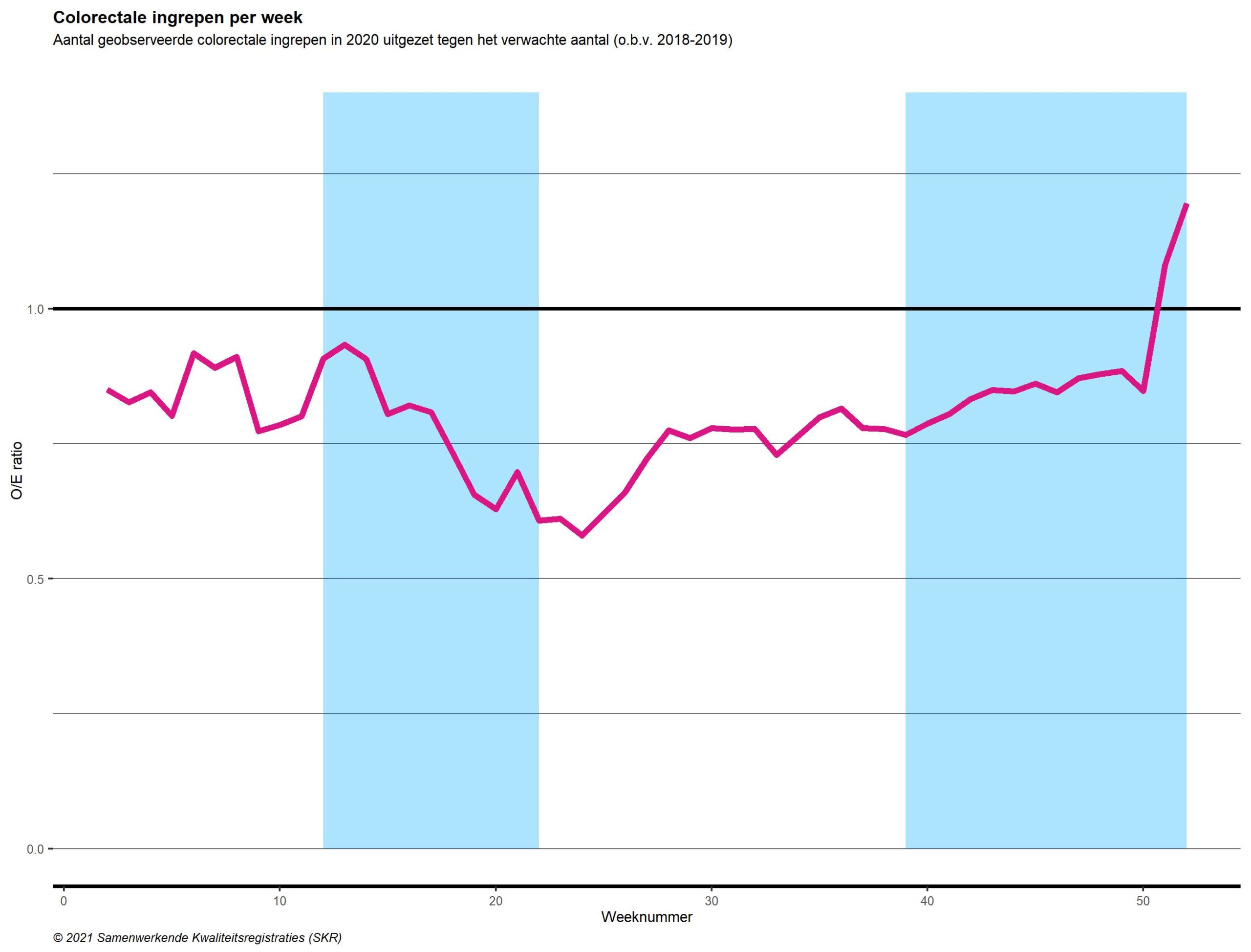
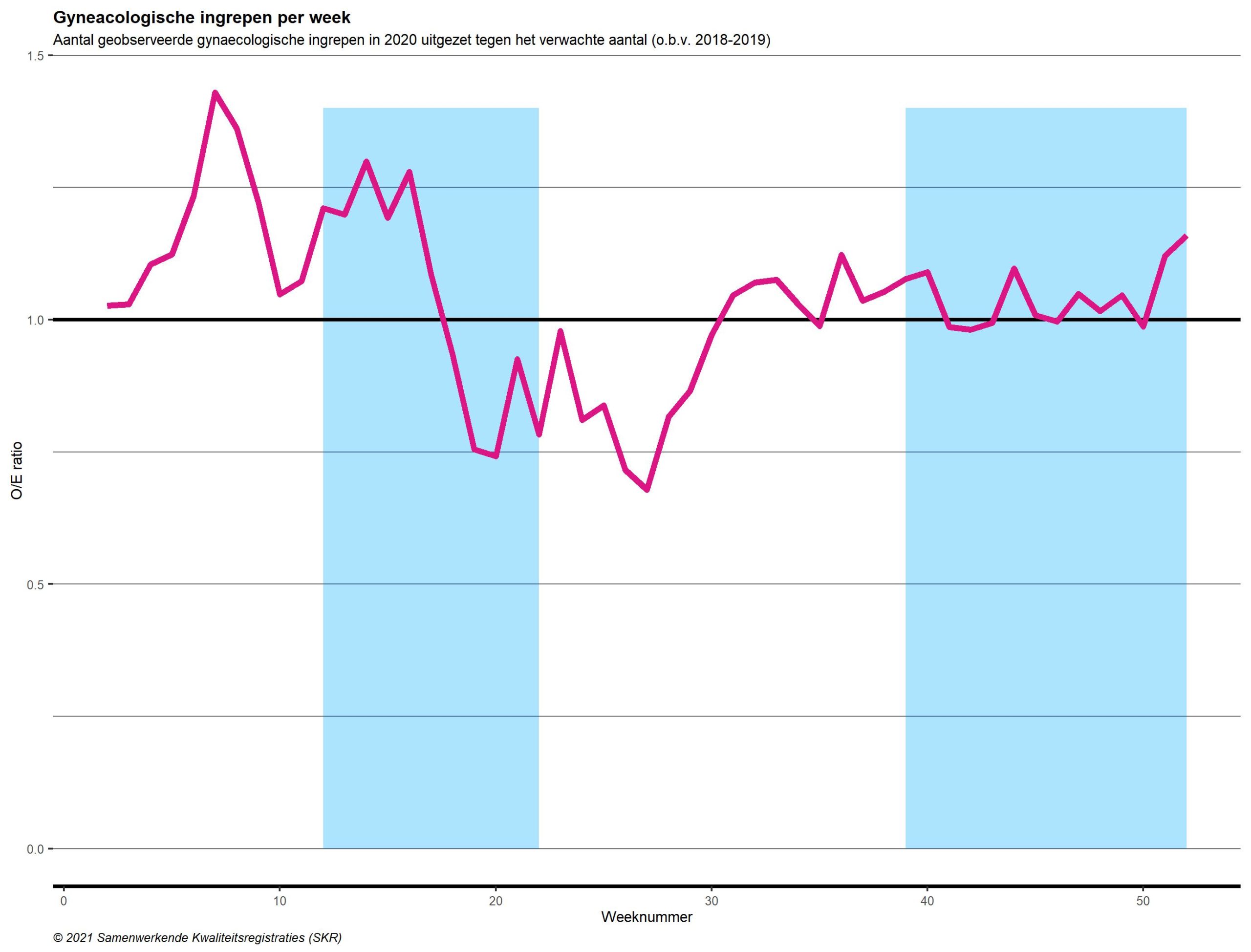
In figuren 3 a,b,c,d is voor verschillende tumorsoorten het aantal verrichte ingrepen in 2020 uitgezet. Dit is gedaan per week, tegen het aantal verwachte ingrepen op basis van de referentieperiode (2018/2019), in een Observed/Expected ratio (O/E ratio) (zie hoofdstuk ‘Opzet Onderzoek’). Het gaat om a) operaties aan de longen b) operaties aan organen in de bovenbuik (slokdarm-, maag-, alvleesklierkanker en leveruitzaaiingen), c) operaties aan de dikke- en endeldarm en d) operaties aan de vrouwelijke geslachtsorganen (eierstokken, baarmoeder, baarmoederhals en vulva).
Hoewel er bij alle tumorsoorten een daling te zien is, zijn er ook duidelijke verschillen tussen de tumorsoorten aanwezig. Met name bij (endel)darmkankeroperaties en longkankeroperaties blijkt de daling en vervolgens de achterstand in uitgevoerde ingrepen groot. Tegelijk lijken de complexe operaties aan de bovenbuik en gynaeco-oncologische operaties te zijn voortgezet.
Een andere opvallende observatie is de piek in aantallen in de laatste twee weken. Deze piek werd veroorzaakt doordat de zorg normaliter (in de referentieperiode in 2018/2019) wordt afgeschaald in de kerstperiode. In 2020 lijkt de zorg in mindere mate te zijn afgeschaald tijdens deze vakantieperiode.
Figuur 3. Aantal complexe oncologische operaties in 2020 voor a) longkanker b) slokdarm-, maag-, alvleesklier en leverkanker c) (endel)darmkanker d) gynaecologische tumoren, afgezet tegen het verwachte aantal o.b.v. 2018-2019
Effect staken bevolkingsonderzoeken
Op 16 maart 2020 besloot het RIVM in opdracht van het Ministerie van VWS per direct de bevolkingsonderzoeken voor borst-, darm- en baarmoederhalskanker tijdelijk te stoppen. Het besluit is genomen om zo in de ziekenhuizen capaciteit vrij te maken voor de COVID-19-zorg. Dat dit waarschijnlijk een groot effect heeft gehad is te zien in figuur 4. De daling in het aantal operaties voor darmkanker, in totaal 21% minder dan in de referentieperiode, werd vooral veroorzaakt door de daling in het aantal patiënten die doorverwezen werden via het bevolkingsonderzoek. Het aantal patiënten doorverwezen via de huisarts vanwege met darmkanker gepaard gaande klachten daalde ook, tot 20% minder begin mei. Het aantal door de huisarts doorverwezen patiënten herstelde zich ook weer in de periode na de eerste golf. Ook in het aantal diagnoses voor baarmoederhalskanker is een dip te zien. De daling in het aantal ingrepen bereikte tijdens de tussenperiode een dieptepunt: slechts 52% van het aantal verwachte ingrepen werd uitgevoerd. Of deze uitstel van de diagnostiek en behandeling de prognose van kankerpatiënten heeft beïnvloed, zal pas in de komende jaren duidelijk worden.
Figuur 4. Aantal colorectale operaties per indicatie: diagnose o.b.v. klachten of via het bevolkingsonderzoek, in 2020 afgezet tegen het verwachte aantal o.b.v. 2018-2019
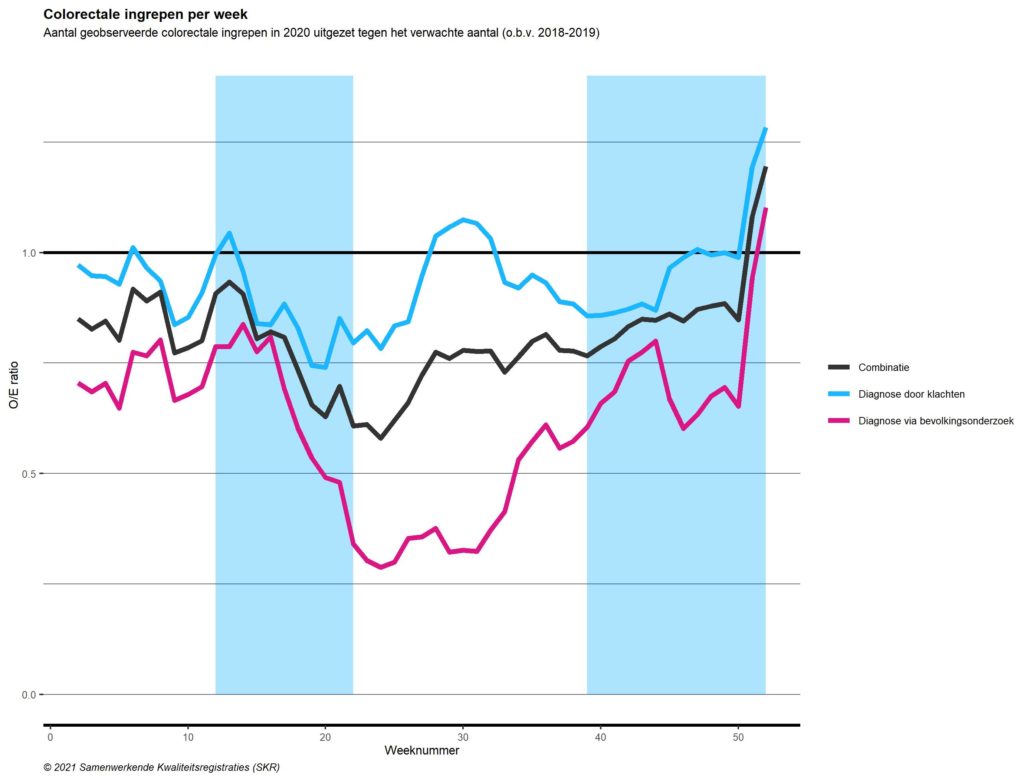
Voorrang oncologie?
Dat er door de druk op het operatieprogramma en op de verpleeg- en IC-afdelingen mogelijk keuzes moesten worden gemaakt in het ziekenhuis (welke operaties konden wel en welke niet doorgaan?), is te zien in figuur 5. Ondanks het feit dat het aantal longkankerdiagnoses afnam tot bijna de helft van wat was verwacht, daalde tijdens de eerste golf het aantal operaties voor longkanker minder dan longoperaties voor goedaardige aandoeningen. Ook in de tweede golf, waarin het aantal longkankerdiagnoses minder daalde dan in de eerste golf, lijken de longchirurgen en artsen opnieuw (gedwongen) voorrang te hebben gegeven aan de longkankeroperaties.
Figuur 5. Aantal longkankerdiagnoses en longoperaties voor maligne versus benigne indicaties in 2020, afgezet tegen het verwachte aantal o.b.v. 2018-2019
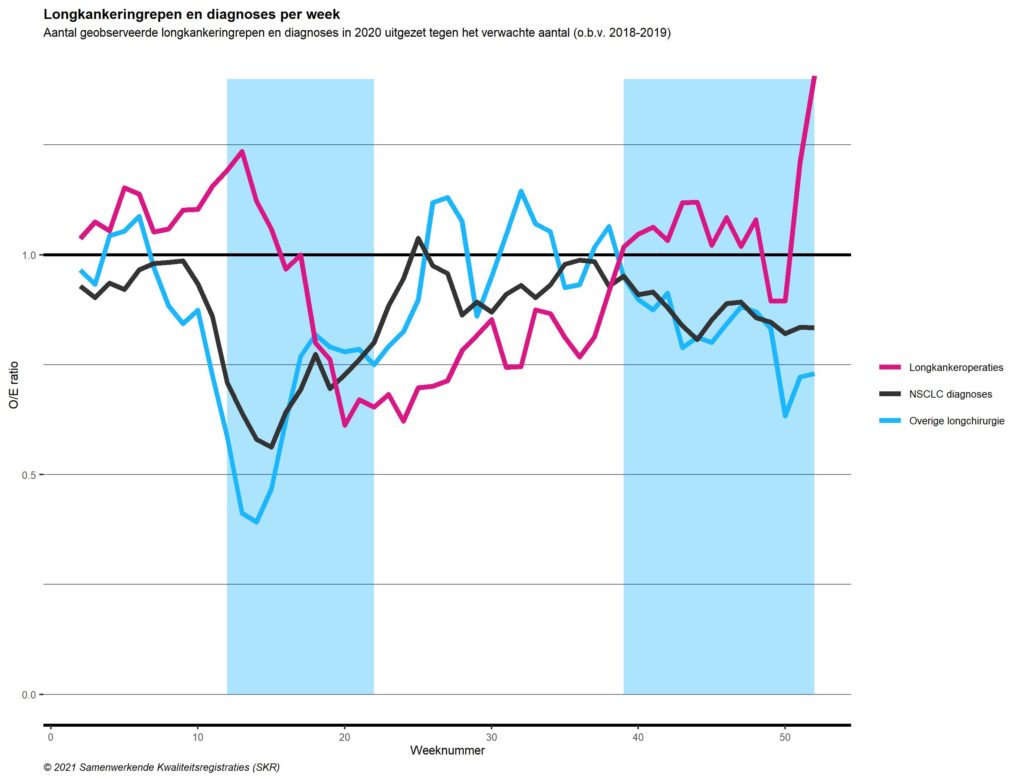
Snellere behandeling voor kankerpatiënten
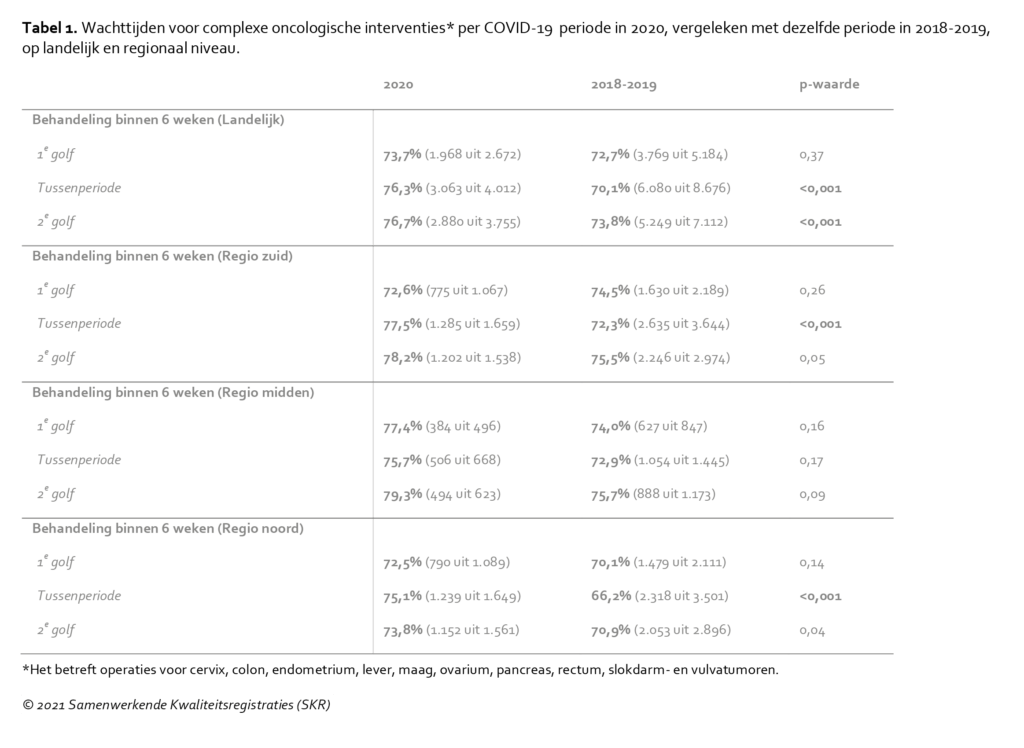
In 2020 bleek de tijd tussen het eerste bezoek aan de polikliniek (of de datum van diagnose) tot de start van de behandeling korter voor patiënten die een complexe oncologische ingreep ondergingen ten opzichte van de referentieperiode. Over het gehele land werden meer patiënten binnen zes weken behandeld in de tussenperiode en de tweede golf dan eerst werd verwacht (Tabel 1). Voor patiënten met leveruitzaaiingen nam de wachttijd in de tussenperiode zelfs met elf dagen af ten opzichte van 2018/2019 (24 versus 35 dagen). In de eerste golf werd dit fenomeen van snellere behandeling niet waargenomen. Patiënten die in de eerste golf een behandeling ondergingen werden ook grotendeels voor de start van de pandemie gediagnosticeerd. Voor patiënten met een primaire maligniteit in het hoofd-hals gebied, was de tijd tot operatieve behandeling zelfs korter tijdens de eerste golf (vijf dagen verschil).
Verschuiving in kenmerken van geopereerde patiënten
In de kwaliteitsregistraties worden kenmerken van de patiënt en de tumor vastgelegd, evenals behandelwijzen. Zoals hierboven beschreven zijn er minder kankerpatiënten gezien in de ziekenhuizen, mogelijk doordat zij niet met hun klachten naar de dokter zijn gegaan. Hierdoor kan de patiëntengroep die chirurgisch behandeld is, veranderd zijn ten opzichte van de referentieperiode. De analyses in tabel 2 laten zien dat er in de tweede golf relatief minder oudere patiënten van boven de 70 jaar chirurgisch zijn behandeld. Ook zijn er minder patiënten met een longziekte als comorbiditeit geopereerd. Dit geldt voor zowel de eerste golf, de tussenperiode als de tweede golf. Dit zouden aanwijzingen kunnen zijn dat bepaalde groepen patiënten, zoals ouderen met een longziekte, een grotere terughoudendheid hadden om met hun klachten naar de dokter c.q. het ziekenhuis te gaan. Dit blijft echter een hypothese. Een andere hypothese is dat er bij kwetsbare patiënten andere (non-chirurgische) behandelkeuzes zijn gemaakt. Denk bijvoorbeeld aan stadium IV-ovariumkanker waar vaker voor systeemtherapie is gekozen in plaats van een operatie om de operatie- en IC-capaciteit te ontzien.

Verandering in behandelkeuzes
Al vrij vroeg tijdens de COVID-19-pandemie kwamen er berichten in de medische literatuur dat patiënten die een coronabesmetting opliepen gedurende het perioperatieve proces een hoge kans hadden op ernstige longcomplicaties (51%) en postoperatieve sterfte (24%) 2. Het is mogelijk dat dit er bij bepaalde patiënten toe heeft geleid dat is afgezien van operatie en te kiezen voor een andere behandeling, zeker wanneer er een goed behandelalternatief is. Zo hoeft deze keuze bijvoorbeeld bij laagstadium longkanker niet per se de kwaliteit van zorg te verminderen (zie paragraaf Radiotherapie).
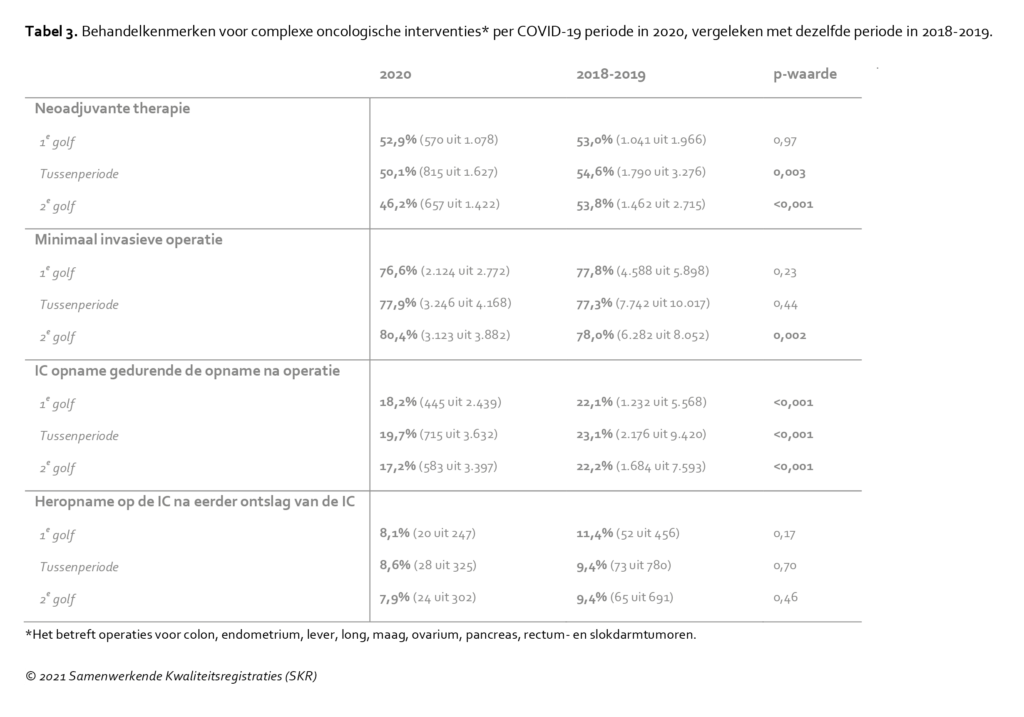
Zoals weergegeven in tabel 3 zijn er tijdens de COVID-19-pandemie andere behandelbeslissingen genomen. Daarbij ging het bijvoorbeeld om radiotherapeutische, systemische (chemotherapie) of een gecombineerde voorbehandeling voorafgaand aan de operatie waarin de tumor werd weggenomen (neo-adjuvante therapie). In 2020 werd er vaker afgezien van zo’n voorbehandeling. Dit is met name zichtbaar voor operaties uitgevoerd in de tussenperiode en de tweede golf; mogelijk hadden de patiënten die in de eerste golf geopereerd werden hun neo-adjuvante behandeling al afgerond. Of het weglaten van neo-adjuvante therapie gevolgen zal hebben voor de lange termijn overleving zal in de toekomst moeten blijken. Anders dan bij andere ziektebeelden is de neoadjuvante therapie voor alvleesklierkanker op niveau gebleven. Dit blijkt onder meer uit het aantal inclusies in de trial naar het effect van neoadjuvante therapie: de PREOPANC-2.
Borstkanker uitgesteld opereren
Ook bij de behandeling van borstkanker zijn opvallende veranderingen te zien in 2020, ten opzichte van de referentieperiode (2018/2019). Anders dan bij andere kankersoorten werd bij borstkanker significant vaker voorafgaand aan de operatie gekozen voor een behandeling met neo-adjuvante therapie. Dit gebeurde zowel tijdens de eerste golf (37% versus 24%) als in de tussenperiode (37% vs 26%). Over de tweede golf is momenteel nog geen data beschikbaar. Het gebruik van neo-adjuvante hormoontherapie steeg bijvoorbeeld van 3,9% in de referentieperiode naar 6,4% tijdens de eerste golf en van 3,8% naar 8,9% tijdens de tussenperiode.
Open of minimaal invasief opereren
Het beeld t.a.v. minimaal invasieve operaties, via een scopische techniek of met de robot, is wisselend voor de verschillende operaties. In het algemeen lijkt er in 2020 geen significante daling te zijn geweest van het (internationaal gezien) hoge percentage minimaal invasieve ingrepen in Nederland (Tabel 3). Tijdens de eerste golf werd bij sommige operaties, zoals die voor alvleesklierkanker, wél bewust afgezien van robotoperaties. Voor dergelijke operaties is doorgaans meer operatietijd nodig; afzien van deze operaties heeft mogelijk de druk op het operatieprogramma vermindert.
Minder opnames op de IC
Voor de complexe oncologische ingrepen die zijn besproken in dit hoofdstuk geldt dat het risico op soms levensbedreigende complicaties aanzienlijk is. Uit voorzorg worden patiënten postoperatief regelmatig opgenomen ter bewaking op de IC, om snel te kunnen handelen bij complicaties. Ook gebeurt het dat na enkele dagen op de verpleegafdeling complicaties optreden, waarvoor de patiënt dan (her)opgenomen moet worden op de IC. Opvallend is dat in alle periodes in 2020 het percentage patiënten opgenomen op de IC significant lager was dan in de referentieperiode. Gebaseerd op data van de maag- en slokdarmkankerregistratie lijkt ook het aantal heropnames op de IC gedaald, hoewel dit niet statistisch significant was (Tabel 3).
Uitkomsten ‘at risk’
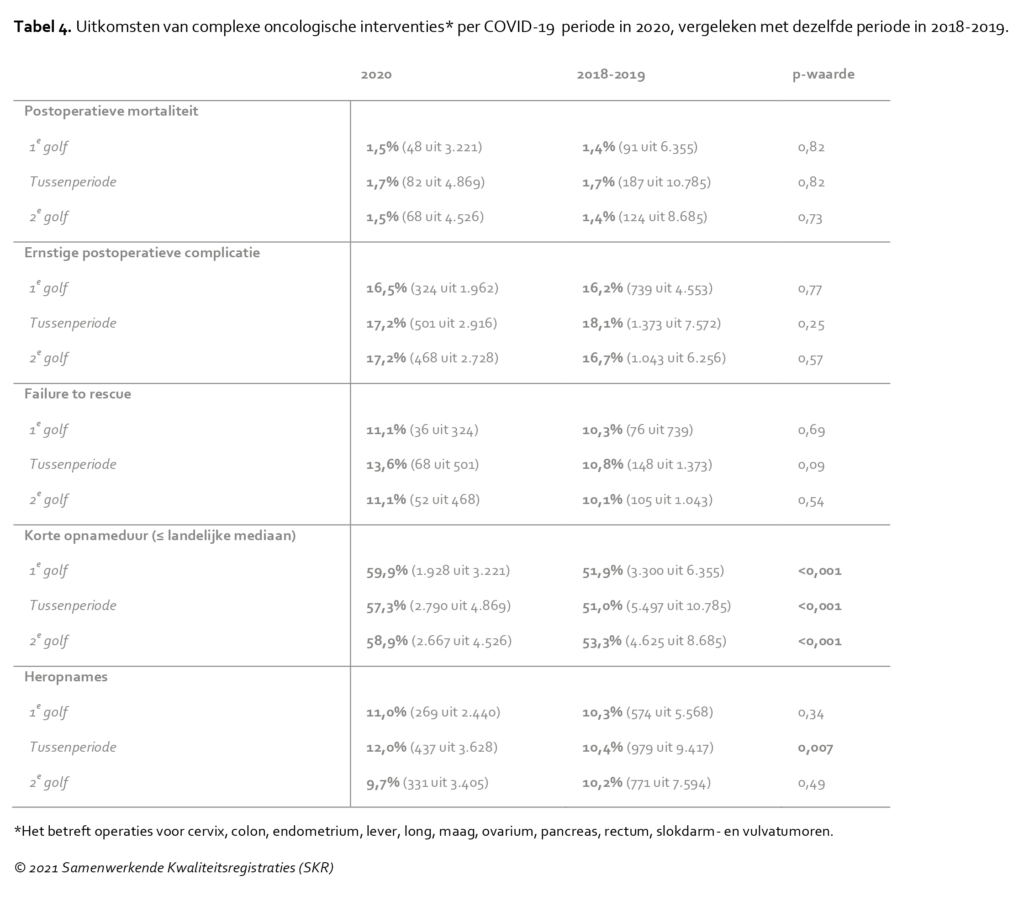
In een situatie waarin het zorgpersoneel onder druk staat en zorg moet verlenen aan zowel COVID-19 als non-COVID-19-patiënten, is het voor te stellen dat de postoperatieve uitkomsten hieronder lijden. Een indicator die gebruikt wordt om de kwaliteit van de postoperatieve zorg te meten is ‘failure to rescue’: het percentage patiënten dat aan ernstige postoperatieve complicaties overlijdt. Uit een gepoolde analyse van elf complexe oncologische operaties in de drie periodes van 2020 blijkt dat, ondanks de lagere IC-opnamepercentages, zowel de postoperatieve complicaties, de postoperatieve sterfte, als de ‘failure to rescue’ niet hoger lag ten opzichte van de referentieperiode (Tabel 4).
Eerder naar huis
Bovendien laten de analyses zien dat patiënten in alle periodes van 2020 eerder uit het ziekenhuis zijn ontslagen (Tabel 4). Dit heeft in de tussenperiode geleid tot een geringe toename van het aantal heropnames in het ziekenhuis. Dit zou gevallen kunnen betreffen waarin de patiënt achteraf bezien toch te vroeg uit het ziekenhuis ontslagen was. De zorg voor patiënten thuis zal mogelijk ook meer druk hebben gelegd op de thuis- en huisartsenzorg, die in coronatijd eveneens onder moeilijke omstandigheden hebben gewerkt.
Bestraling
Voor sommige tumorsoorten geldt dat bestraling (radiotherapie) een belangrijke rol heeft in de primaire behandeling van de tumor. Dit geldt bijvoorbeeld voor niet-kleincellige longkanker (NSCLC), waarmee in Nederland jaarlijks bijna 10.000 mensen gediagnosticeerd worden.
Minder diagnoses longkanker
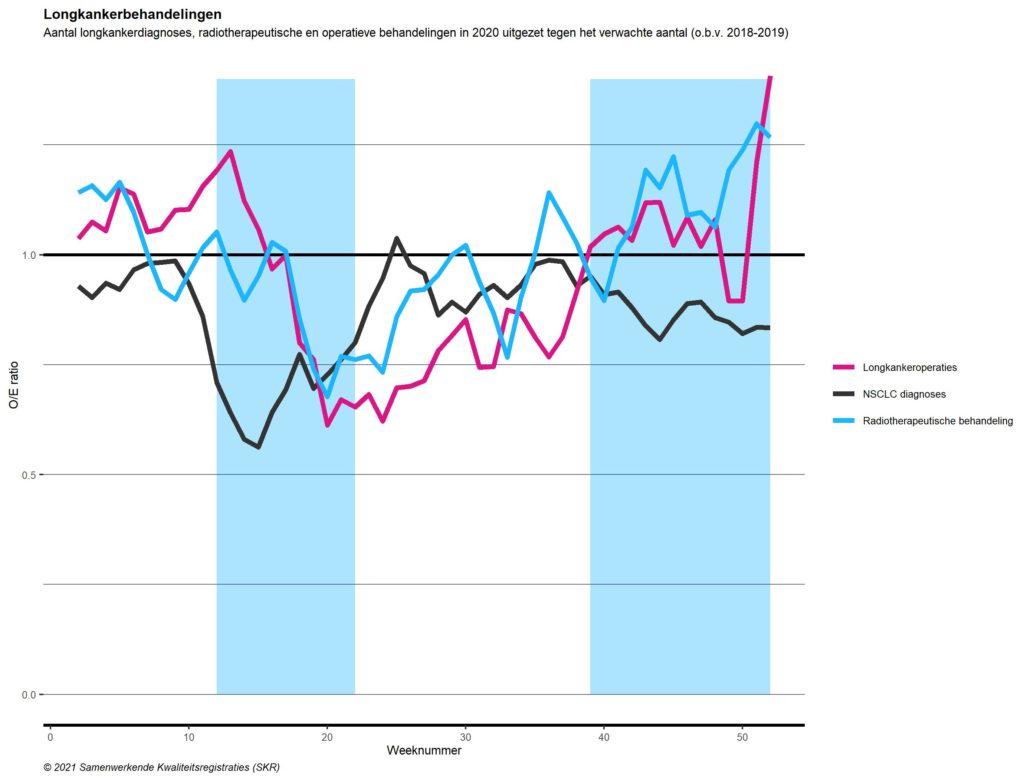
Tijdens de COVID-19 pandemie was er een markante daling in het aantal diagnoses van niet-kleincellige longkanker. Deze daling werd tijdens de eerste golf logischerwijs gevolgd door een afname van 12% aan bestralingsbehandelingen (Figuur 6). Een dalende trend was in deze periode ook te zien voor het aantal longkankeroperaties. Hierna steeg het aantal bestralingen in de tussenperiode en vonden er tijdens de tweede golf juist 11% meer behandelingen plaats. Ondanks een aanzienlijke daling in het aantal longkankerdiagnoses tijdens de COVID-pandemie hebben er in totaal slechts 3% minder bestralingen plaatsgevonden voor niet-kleincellige longkanker.
Figuur 6. Aantal longkankerdiagnoses (NSCLC), longoperaties en -bestralingen in 2020, afgezet tegen het verwachte aantal o.b.v. 2018-2019
Regionale verschillen
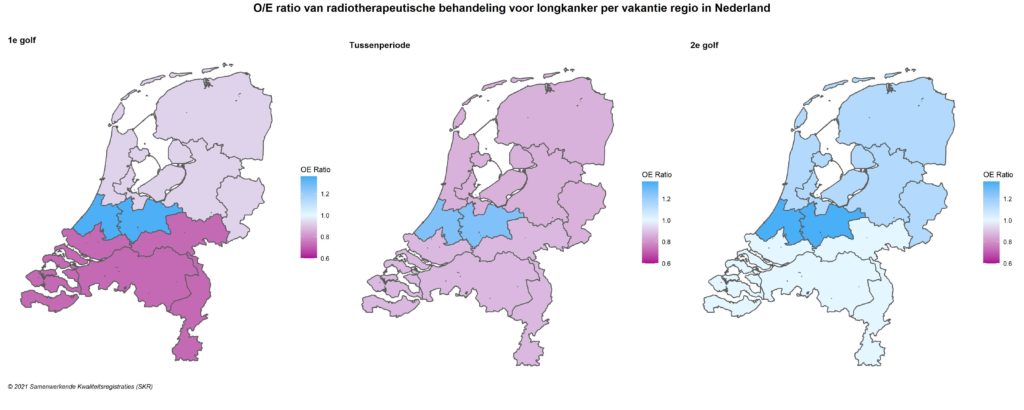
Ook bij de radiotherapie voor longkanker zijn verschillen te zien tussen de regio’s in het land (Figuur 7). Zo is er vooral in de regio Zuid gedurende de eerste golf en de tussenperiode minder bestraald, terwijl er met name in Midden Nederland relatief meer patiënten zijn behandeld. We zien ook dat de achterstand in regio Zuid in de loop van 2020 nauwelijks is ingehaald, terwijl dat in de noordelijke regio wel enigszins het geval was.
Figuur 7. Regionale verschillen in curatieve bestralingsbehandelingen voor longkanker in de regio’s Noord-, Midden, Zuid-Nederland in 2020, afgezet tegen het verwachte aantal o.b.v. 2018-2019
Behandelkeuzes
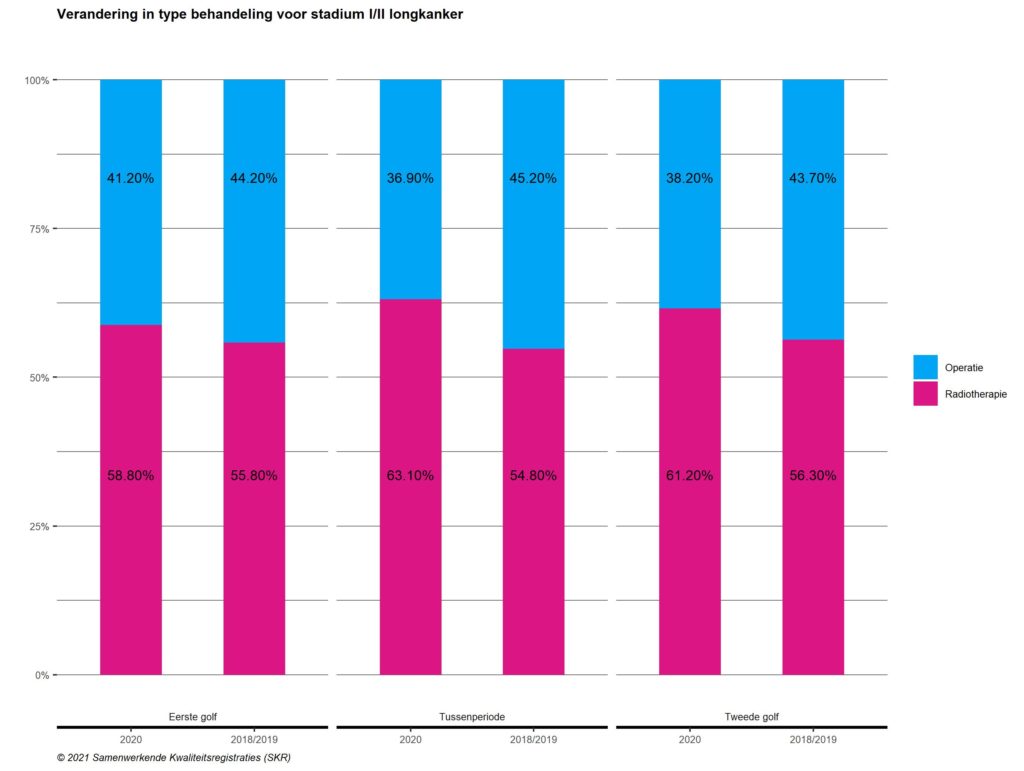
Patiënten die zijn behandeld voor een vroeg stadium NSCLC zijn in 2020 verhoudingsgewijs vaker stereotactisch bestraald dan geopereerd, in vergelijking met de referentieperiode (Figuur 8). In de eerste golf werd 59% van de vroeg stadium tumoren behandeld met bestraling terwijl dit in de referentieperiode 56% was. In de tussenperiode steeg het percentage radiotherapeutische behandelde patiënten van 55% naar 63%. In de tweede golf steeg dit percentage van 56% naar 61%. Het kan zijn dat meer patiënten voor bestraling kozen, omdat zij daarvoor niet in het ziekenhuis opgenomen hoefden te worden. Ook de druk op het operatieprogramma en de IC voor de postoperatieve zorg kan een rol gespeeld hebben in deze verandering in behandelingskeuze.
Voor patiënten met stadium III niet-kleincellig longcarcinoom is een combinatie van chemotherapie en bestraling (soms gevolgd door chirurgie) de meest effectieve behandelingsoptie. Nadeel is dat de behandeling erg belastend kan zijn voor de patiënt en deze tijdelijk in een kwetsbare conditie kan brengen, zeker wanneer de behandelingen gelijktijdig worden gegeven (concurrent). Tijdens de eerste golf werden patiënten minder vaak behandeld met chemoradiotherapie dan werd verwacht op basis van de referentieperiode (73% in 2020 versus 85% in 2018/2019) Als er chemoradiotherapie werd gegeven, was het sequentiële aandeel relatief groter in 2020 dan in de referentieperiode. In 2020 werd in de eerste golf in 28% sequentieel behandeld, tegen 21% in 2018/2019.
Figuur 8. Verhouding tussen het percentage patiënten behandeld voor stadium I-II NSCLC met een operatieve resectie versus stereotactische bestraling in 2020, afgezet tegen het verwachte percentage o.b.v. 2018-2019
Immunotherapie en doelgerichte behandelingen
Al op 22 maart 2020 publiceerde de Nederlandse Vereniging voor Medische Oncologie (NVMO) op haar website een ‘handvat COVID-19 oncologie’. Aanleiding vormden de vele vragen vanuit de beroepsgroep van oncologen over het al dan niet starten of laten doorgaan van systemische behandelingen, zoals chemo-, immuno- en doelgerichte therapieën3. Op dat moment was er een groot gemis aan wetenschappelijke data over de verhoogde vatbaarheid van kankerpatiënten tijdens hun behandeling voor COVID-19. Het maken van de afweging tussen de noodzakelijke kankerbehandeling en de risico’s van een COVID-19-infectie bij deze kwetsbare patiëntengroep was niet gemakkelijk. Het handvat adviseerde om in ieder geval terughoudend te zijn met immuun checkpoint inhibitoren (ICI) en deze waar mogelijk te vervangen door doelgerichte therapie.
Uitgezaaid melanoom
Patiënten met een uitgezaaid melanoom (stadium III-IV) komen in aanmerking voor een behandeling met immunotherapie (ICI). Dit kan het geval zijn na een operatie waarbij alle tumor is weggenomen (adjuvante setting) dan wel zonder operatie wanneer de tumor is uitgezaaid naar de organen, zoals de hersenen, lever of longen, waardoor de tumoren niet meer volledig weg te halen zijn (irresectabele setting). Beide patiëntengroepen worden behandeld in veertien melanoomcentra in Nederland, die gezamenlijk een registratie bijhouden van alle patiënten die naar hen verwezen worden met uitgezaaid melanoom. Figuur 9 laat zien dat het aantal patiënten dat verwezen werd naar de melanoomcentra aanzienlijk daalde tijdens de eerste golf en opnieuw daalde tijdens de tweede golf.
Figuur 9. Aantal stadium III-IV melanoompatiënten behandeld in een adjuvante of irresectabele setting in 2020, afgezet tegen het verwachte aantal o.b.v. 2019
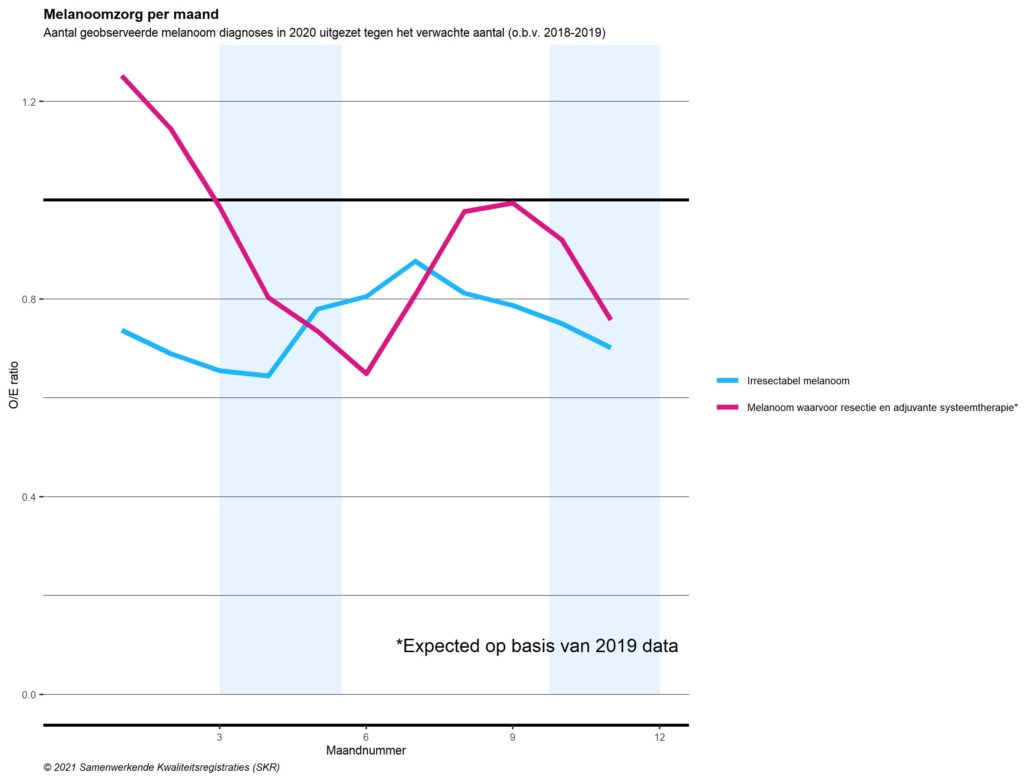
Verschil tussen adjuvant en irresectabel
Patiënten die een naar de organen uitgezaaid melanoom hebben, hebben slechte overlevingskansen. Bij dergelijke patiënten is een resectie van het melanoom vaak niet zinvol. De laatste jaren is de overleving gelukkig verbeterd door de introductie van immuno- en doelgerichte therapieën4. Ook wordt sinds december 2018 al in een eerder stadium, wanneer de uitzaaiingen nog chirurgisch te verwijderen zijn, aanvullende immunotherapie toegepast (adjuvante therapie). Hierdoor neemt het percentage patiënten af dat vervolgens een irresectabel melanoom krijgt en daarvoor behandeld moet worden. Deze bevindingen zien we in figuur 9 weergegeven. Gedurende het hele jaar 2020 lijkt het aantal irresectabele/naar de organen uitgezaaid melanoompatiënten afgenomen te zijn, met mogelijk een lichte daling tijdens de eerste en tweede golf en een stijging in de tussenperiode. Voor de patiënten die een aanvullende behandeling (adjuvante therapie) zouden moeten ondergaan, is de mogelijke invloed van de COVID-19-pandemie echter veel duidelijker aanwezig. Tijdens de eerste golf is er sprake van een scherpe daling van het aantal patiënten dat met aanvullende immunotherapie behandeld werd, met een tijdelijk herstel in de tussenperiode waarna er opnieuw een daling optrad in de tweede golf. Deze daling wordt in alle regio’s gezien, maar is in Zuid Nederland het sterkst. Mogelijk is er bij meer patiënten afgezien van adjuvante behandeling. Een deel van dit effect zou ook te maken kunnen hebben met de afname van het aantal patiënten dat landelijk gediagnosticeerd is met huidkanker5. Hierdoor zouden dus ook de primaire melanomen met (microscopische) uitzaaiingen in de lymfeklieren nog niet ontdekt kunnen zijn.
Uitgebreidere melanomen
Voor wat betreft de algemene karakteristieken van de patiënten met irresectabel/uitgezaaid melanoom, zien we vooral tijdens de tweede COVID-golf dat zij een ongunstigere uitgangssituatie lijken te hebben (Tabel 5): patiënten hebben een slechtere conditie (ECOG-performance score), hogere tumormarkers (LDH-levels) en hogere tumorstadia (AJCC stage) dan in de referentieperiode. Het meest opvallende verschil is het hogere percentage patiënten met hersenuitzaaiingen in de tweede golf (40% versus 27% in de referentieperiode). Dit verschil is een stuk minder uitgesproken tijdens de eerste COVID-golf en de tussenperiode (32% en 30% tegenover 29% en 27% in de referentieperiodes). Dit lijkt ook geleid te hebben tot ‘zwaardere behandelingen’ voor patiënten in de tweede golf, met een toegenomen gebruik van combinatie immunotherapie: 40% versus 25% in de referentieperiode.

Bijwerkingen
Wanneer melanoompatiënten behandeld worden met systeemtherapie kan dit gepaard gaan met toxiciteiten (bijwerkingen) van de middelen. Deze toxiciteiten treden meestal niet direct op, maar na een aantal weken of maanden. Omdat de toxiciteiten dus mogelijk nog niet zijn opgetreden bij patiënten die tijdens de tussenperiode en de tweede golf zijn behandeld, is er in dit onderzoek alleen gekeken naar de eerste COVID-golf.
Wat hierbij opvalt is dat er minder toxiciteiten zijn geregistreerd: voor adjuvante therapie 8.5% van de behandelde patiënten versus 17.1% in de referentieperiode en voor irresectabele ziekte 18% versus 23% in de referentieperiode (2018/2019). Minder patiënten werden opgenomen in verband met toxiciteit: adjuvant 5.9% versus 9.2% en irresectabel 8% versus 14% in de referentieperiode. Het is het meest waarschijnlijk dat patiënten tijdens de COVID-19-perioden minder vaak het ziekenhuis hebben bezocht met klachten passend bij de bijwerkingen van hun therapie; mogelijk is ook minder vaak de beslissing genomen om hen daarvoor op te nemen, gezien de situatie in het ziekenhuis.
Beschouwing
De COVID-19 pandemie lijkt een aanzienlijke impact te hebben gehad op de oncologische zorg in 2020. Dit geldt vooral voor het aantal gestelde diagnoses, maar in minder mate ook in de keuzes voor de behandeling van kankerpatiënten. Voor sommige diagnoses, zoals die van longkanker, daalde het volume tijdens de eerste golf tot bijna de helft van wat er op basis van historische gegevens verwacht zou worden. Bovendien werden er in 2020 in totaal 2000 complexe oncologische operaties minder uitgevoerd. Dit zou mogelijk het gevolg kunnen zijn van uitgestelde diagnoses, zoals het stoppen van de bevolkingsonderzoeken.
De ziekenhuiszorg heeft soms (noodgedwongen) geanticipeerd op de grote druk op de operatie-, intensive care en verpleegafdelingen. Al vroeg in de pandemie is er een piek in complexe oncologische operaties gezien, voorafgaand aan de eerste golf. Dit is mogelijk een uiting van het feit dat chirurgische teams anticipeerden op de schaarste aan operatie- en IC-capaciteit die eraan zat te komen. Ook zijn er in 2020 andere keuzes gemaakt in de behandeling van patiënten, bijvoorbeeld door een andere operatieve benadering te kiezen. Denk hierbij aan het afzien van een operatie met de robot, om lange operatietijden te voorkomen. Patiënten gingen postoperatief minder vaak naar de (soms overvolle) IC, waardoor er complexere zorg op de verpleegafdelingen geleverd zal zijn. Ook zijn patiënten gemiddeld iets eerder naar huis ontslagen, met als mogelijk gevolg dat er weer meer nazorg in de eerste lijn geleverd moest worden. Tevens zijn er tekenen dat er in de ziekenhuizen soms voorrang is gegeven aan de oncologie ten opzichte van patiënten met benigne diagnoses, beslissingen met mogelijk een grote impact op het leven van patiënten (zie hiervoor ook het hoofdstuk electieve zorg).
Het lijkt erop dat er in 2020 soms ook gekozen is voor een goed behandelalternatief (mits voorhanden), waardoor een operatie kon worden uitgesteld of afgezegd. Een voorbeeld hiervan is de inzet van hormonale therapie bij borstkanker en stereotactische bestraling bij laagstadium longkanker. Ook lijken er soms andere behandelkeuzes gemaakt te zijn bij patiënten in een kwetsbare conditie, bijvoorbeeld door een bijkomende longziekte.
Daarentegen zijn er soms weer beslissingen genomen om patiënten niet in een kwetsbare conditie te brengen, door een neo-adjuvante behandeling met chemotherapie achterwege te laten, bestralingsschema’s aan te passen (sequentieel i.p.v. concurrent) of behandelingen met immunotherapie tijdelijk te staken. De kwaliteit van zorg in het ziekenhuis lijkt, voor zover wij nu kunnen analyseren, hier niet onder geleden te hebben: er waren acceptabele wachttijden, niet meer bijwerkingen, complicaties of overlijden aan complicaties. Dit is een majeure prestatie van het ziekenhuispersoneel, dat ondanks alle druk op de afdelingen en risico’s van coronabesmettingen veilige zorg is blijven leveren aan oncologische patiënten.
Dit hoofdstuk suggereert dat er een behoorlijk aantal kankerdiagnoses is uitgesteld. Als dit daadwerkelijk zo is, dan is dit een grote zorg. Bij sommige tumorsoorten lijken zich nu al patiënten te presenteren met verder gevorderde ziekte. Dit betreft bijvoorbeeld patiënten met uitgezaaid melanoom en longkanker. Mogelijk zou dit hun prognose kunnen beïnvloeden. Ook lijken er regionale verschillen te zijn in de mate waarin achterstanden in diagnoses en behandelingen zijn ontstaan gedurende het jaar 2020 en de mate waarin deze weer ingehaald konden worden. Vervolgonderzoek zal moeten aantonen in hoeverre dit consequenties heeft of heeft gehad voor de diagnose, behandeling en (kwaliteit van) de overleving van deze groep oncologische patiënten, bij wie de diagnose nog gesteld moet worden.
Referenties
- https://www.palga.nl/nieuws/door-de-covid-19-crisis-zijn-er-nu-minder-kankerdiagnoses-hoe-beperken-we-de-impact.html].
- COVIDSurg collaborative. Mortality and pulmonary complications in patients undergoing surgery with perioperative SARS-CoV-2 infection: an international cohort study. Lancet 2020; 396: 27–38
- https://www.nvmo.org/dossier-covid-19/handvat-covid-19-oncologie-2-0/
- van Zeijl MCT et al. Survival outcomes of patients with advanced melanoma from 2013 to 2017: Results of a nationwide population-based registry. Eur J Cancer. 2021; 144:242-251.
- Uyl-de Groot CA et al. [Fewer cancer diagnoses during the COVID-19 epidemic according to diagnosis, age and region]. TSG – Tijdschr voor gezondheidswetenschappen. 2020:1-8.
Welke kwaliteitsregistraties hebben bijgedragen aan dit hoofdstuk?
Dutch Institute for Clinical Auditing (DICA)
In dit hoofdstuk wordt (gepoolde) data gepresenteerd van verschillende oncologische DICA-registraties. Er wordt data gepresenteerd van de:
- Dutch ColoRectal Audit (colorectaal carcinoom)
- Dutch Gynaecological Oncology Audit (endometrium, cervix, vulva en ovarium carcinoom)
- Dutch HepatoBiliary Audit (levermetasten)
- Dutch Head and Neck Audit (hoofd-hals tumoren)
- Dutch Lung Cancer Audit – Lung Oncology (systemische behandeling van longkanker)
- Dutch Lung Cancer Audit – Radiotherapy (radiotherapeutische behandeling van longkanker)
- Dutch lung Cancer Audit – Surgery (chirurgische behandeling van longkanker)
- Dutch Melanoma Treatment Registry (systemische behandeling van melanomen)
- Dutch Pancreatic Cancer Audit (alvleesklierkanker)
- NABON Breast Cancer Audit (borstkanker)
- Dutch Upper Gastrointestinal Cancer Audit (maag- en slokdarmkanker)
In deze registraties wordt (tenzij anders aangegeven) de chirurgische behandeling van de tumortypen geregistreerd. Aangezien het oncologische operaties betreft zijn dit semi-electieve operaties. Spoedoperaties aan colorectale tumoren worden in het acute cluster beschreven.