Een groot deel van de ziekenhuiszorg betreft zorg voor patiënten met chronische aandoeningen zoals diabetes mellitus, astma en chronische nierziekten. Door de vergrijzing zal dit alleen maar toenemen. De impact van de COVID-19-pandemie op de chronische zorg is minder direct meetbaar dan voor acute aandoeningen. Uitstel van zorg kan echter op de lange termijn leiden tot verslechtering van de gezondheidstoestand en tot complicaties. In dit hoofdstuk beschrijven we de gevolgen, voor zover nu bekend, voor diabetespatiënten die zijn behandeld in de tweede en derde lijn en patiënten behandeld met chronische dialyse. Ook wordt de impact van de pandemie op de transplantatiezorg beschreven.
DIABETESZORG
In Nederland worden naar schatting 185.000 patiënten met diabetes mellitus behandeld in de tweede of de derde lijn1 een aantal dat naar verwachting toe zal nemen als gevolg van overgewicht en vergrijzing. Diabetes mellitus is een belangrijke veroorzaker van cardiovasculaire comorbiditeiten en complicaties. Ook is het één van de meest voorkomende oorzaken van nierfalen.2 Daarnaast zorgt deze aandoening voor een lagere levensverwachting en een verminderde kwaliteit van leven.3
Inzicht in Nederlandse diabeteszorg
In Nederland is informatie over de prevalentie en uitkomsten van diabetes mellitus in de populatie voornamelijk gebaseerd op huisartsendatabases die informatie geven over diabetespatiënten in de eerste lijn. Over poliklinisch behandelde diabetespatiënten is echter veel minder bekend, terwijl het verloop en de behandeling van deze ziekte, het zorggebruik en behoeften anders zijn in deze groep, die onder andere alle patiënten met type 1 diabetes omvat.
Daarom is in 2017 DPARD (Dutch Pediatric and Adult Registry of Diabetes) opgericht, een landelijke kwaliteitsregistratie van patiënten met diabetes mellitus, behandeld in de tweede en derde lijn. In DPARD worden zowel kinderen als volwassenen geregistreerd. Data worden niet handmatig geregistreerd, maar direct uit het elektronisch patiëntendossier (EPD) gehaald, waarbij ziekenhuizen minimaal één keer per jaar data aanleveren. DPARD is een beginnende registratie, waarbij rekening moet worden gehouden met de generaliseerbaarheid van de aangeleverde gegevens en de datakwaliteit, die overigens wel elk jaar toeneemt. Om de datakwaliteit te verbeteren zijn in 2020 onder andere de inclusiecriteria voor DPARD duidelijker gedefinieerd, wat van invloed kan zijn op de gerapporteerde patiëntenaantallen.
Basiskarakteristieken
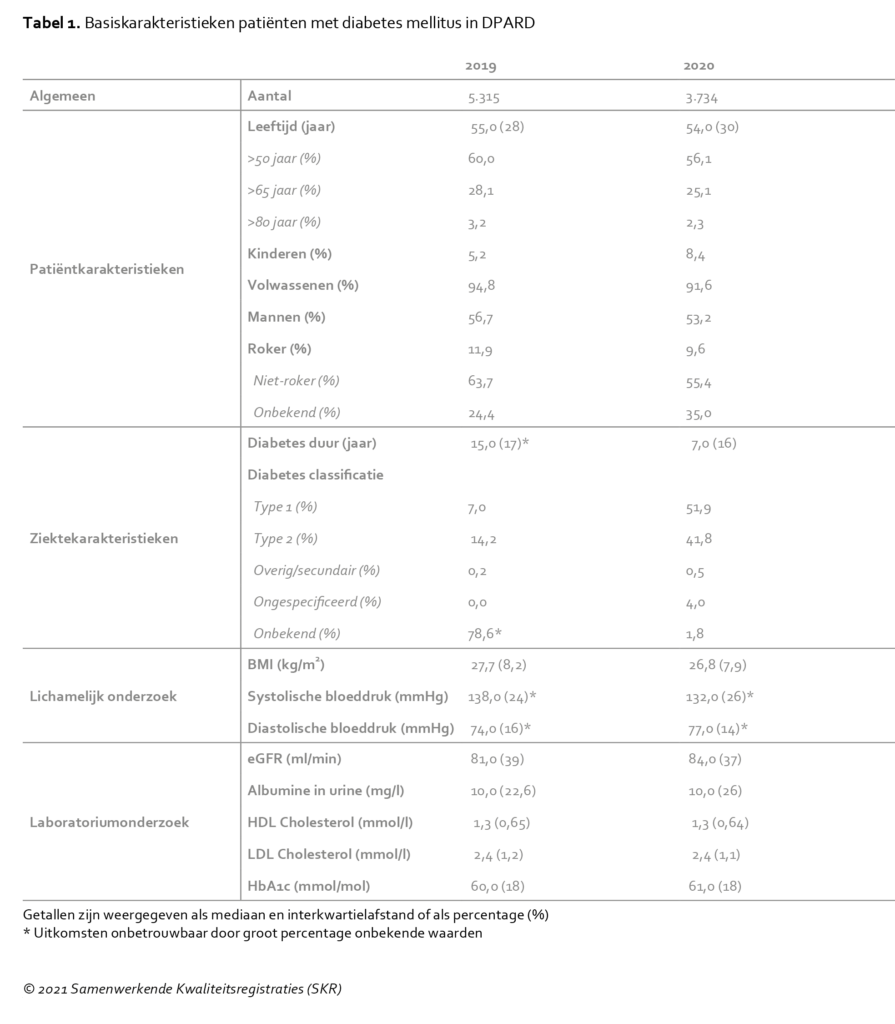
In tabel 1 zijn de patiënt-, ziekte- en diagnostische karakteristieken weergegeven van patiënten met diabetes mellitus in DPARD over de jaren 2019 en 2020. Vijf ziekenhuizen uit Noord-Holland, Utrecht en Friesland hebben data aangeleverd voor beide jaren. De data zijn weergegeven per jaar en niet per periode tijdens de COVID-19 epidemie, omdat informatie van elke patiënt op jaarbasis beschikbaar is en niet per periode. De status van het tabaksgebruik en het lichamelijk onderzoek worden door de zorgverlener handmatig ingevoerd in het EPD. Hierdoor neemt de kans op missende data toe en hebben deze gegevens grotere aantallen onbekenden. De laboratoriumwaarden worden automatisch vastgelegd in een vast format en zijn door alle ziekenhuizen in DPARD aangeleverd.
Aantal poliklinische bezoeken mogelijk lager in 2020
Het is belangrijk om te realiseren dat de getallen afkomstig zijn uit vijf ziekenhuizen in drie provincies, waardoor de resultaten beperkt te generaliseren zijn naar de landelijke situatie. Opvallend is dat het aantal patiënten met diabetes mellitus dat in 2020 door de vijf ziekenhuizen in DPARD geregistreerd werd, lager was dan in 2019. Dit zou kunnen betekenen dat in 2020 minder patiënten op de polikliniek gecontroleerd zijn voor diabetes mellitus dan het voorgaande jaar. Dit kan een vingerwijzing zijn dat dit in Nederland is gebeurd, echter op basis van uitsluitend deze data kan dit niet worden vastgesteld.
Vergelijkbare patiënt-, ziekte- en diagnostische karakteristieken tussen 2019 en 2020
De patiënt- ziekte- en diagnostische karakteristieken zijn vergelijkbaar tussen de patiënten die in 2019 en 2020 in DPARD geregistreerd werden. De gevonden verschillen in type diabetes mellitus en duur van diabetes onder patiënten in het DPARD-cohort zijn mogelijk beïnvloed door het hoge aantal onbekende waarden in 2019. De BMI was vergelijkbaar tussen 2019 en 2020, evenals de laboratoriumwaarden in tabel 1.
Glucoseregulatie diabetespatiënten
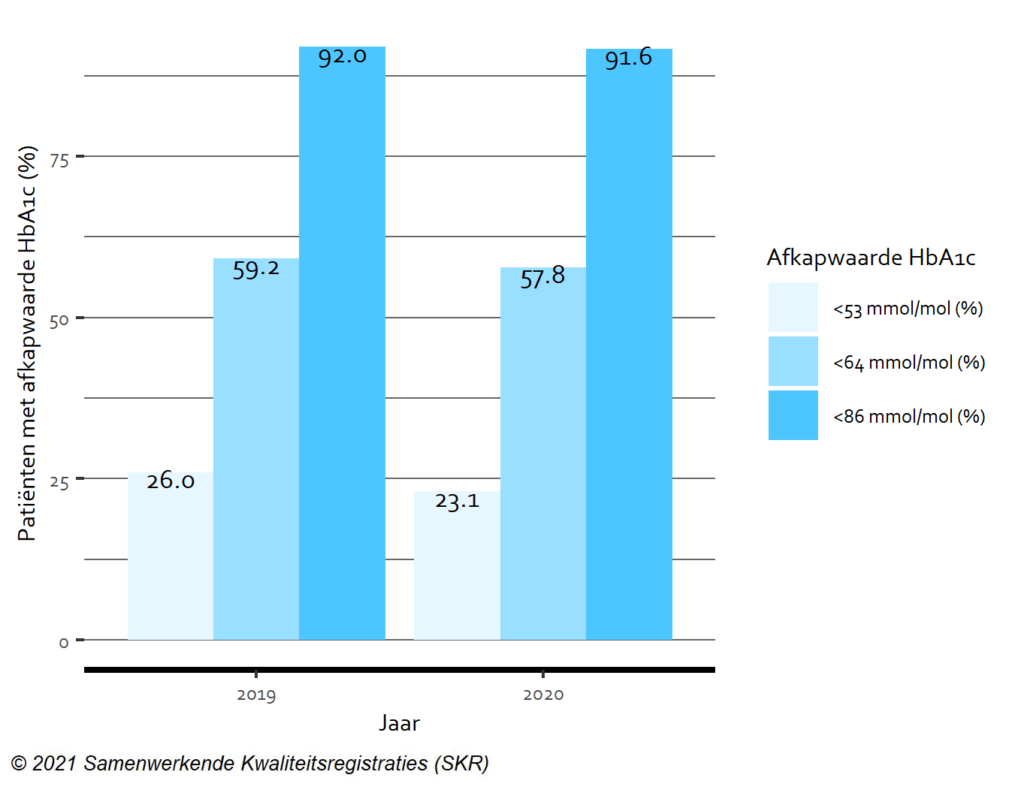
De mediane HbA1c-waarden van de patiënten in DPARD zijn vergelijkbaar tussen 2019 en 2020. Zoals weergegeven in figuur 1 is het percentage patiënten met een HbA1c <53 mmol/mol lager in 2020. Het aantal patiënten met een HbA1c van 86mmol/mol of hoger is vergelijkbaar tussen 2019 en 2020 (respectievelijk 8,0 en 8,3%). Het aantal onbekende HbA1c-waarden is met 7,5% licht toegenomen ten opzichte van 2019 (3,4%). De oorzaak van deze stijging is onduidelijk. Mogelijk is het HbA1c daadwerkelijk minder bepaald, omdat patiënten minder vaak naar het ziekenhuis zijn gekomen vanwege bijvoorbeeld COVID-19 , of werden de bepalingen verricht in een ander ziekenhuis of bij de huisarts. Daarnaast is er voor het jaar 2020 geen informatie beschikbaar van de patiënten, die in 2019 de polikliniek bezochten en in 2020 niet. Dat de patiëntkenmerken in beide jaren vergelijkbaar zijn, suggereert dat dit weinig invloed heeft op de uitkomsten. Dit kunnen we echter niet uitsluiten.
Figuur 1. Glucoseregulatie diabetespatiënten in DPARD
Belang van landelijke registratie
Diabetes mellitus is een belangrijke oorzaak van cardiovasculaire comorbiditeiten en complicaties. Ook is het één van de meest voorkomende oorzaken van nierfalen. DPARD laat zien dat poliklinische populatie gegevens bij diabetes mellitus waardevolle data opleveren.
Het aantal poliklinisch gecontroleerde patiënten met diabetes mellitus in de vijf DPARD-ziekenhuizen leek in 2020 lager ten opzichte van 2019. Mogelijk zorgde COVID-19 voor deze verandering, dit blijft vooralsnog echter onduidelijk. Op basis van de gegevens van deze vijf ziekenhuizen kunnen geen conclusies getrokken worden op nationaal niveau. Het aandeel patiënten met redelijk tot goed gereguleerde diabetes mellitus (HbA1c <53 mmol/mol) was in 2020 lager dan in 2019, terwijl het aantal slecht gereguleerde diabetespatiënten (HbA1c >86 mmol/mol) gelijk gebleven is. Dit zou kunnen betekenen dat minder frequente controles hebben geleid tot een slechtere glucoseregulatie. De Body Mass Index van alle patiënten in DPARD is vergelijkbaar ten opzichte van 2019. DPARD is een jonge registratie, die door haar korte bestaan alleen resultaten op relatief korte termijn laat zien. De DPARD-registratie zal in de toekomst waardevolle data over langere termijn genereren. Diabetes mellitus is een chronische ziekte, waarbij de effecten op laboratoriumuitkomsten, complicaties en comorbiditeit zich pas na jaren openbaren. De impact van de COVID-19-epidemie op de lange termijn zal in de komende jaren verder worden vervolgd. Dit onderstreept het belang van een landelijke diabetesregistratie des te meer, zodat we beter inzicht krijgen in de Nederlandse poliklinisch gecontroleerde patiëntenpopulatie met diabetes mellitus.
DIALYSEZORG
Renine is de Nederlandse registratie van patiënten met chronische nierfunctievervangende therapie. Patiënten worden gevolgd vanaf start dialyse of niertransplantatie tot overlijden. Sinds maart 2020 wordt COVID-19 bij patiënten met chronische dialyse in Renine geregistreerd. Sinds februari 2021 is de registratie uitgebreid met gegevens over vaccinaties tegen COVID-19.
Minder instroom oudere patiënten tijdens eerste golf
Tijdens de COVID-19-pandemie is de zorg voor patiënten met chronische dialyse gecontinueerd en er zijn geen duidelijke effecten op de omvang en samenstelling van de prevalente dialysepopulatie. Eind 2020 stonden er 6.261 chronische dialysepatiënten geregistreerd in Renine, tegen 6.293 patiënten aan het eind van 2019. De kenmerken van de patiëntenpopulatie wijken niet af van voorgaande jaren. De gemiddelde leeftijd in 2020 was 67 jaar en de populatie bestond voor 60% uit mannen. Ruim 20% van de dialysepopulatie heeft diabetes mellitus als primaire oorzaak van de nierziekte.
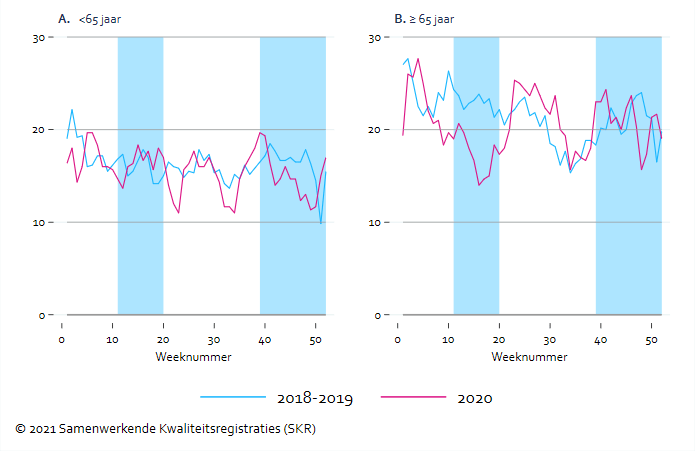
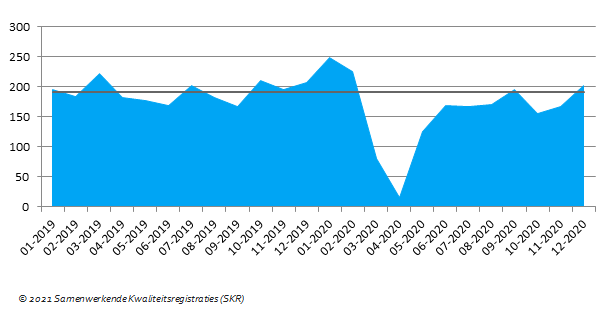
In 2020 zijn 1.664 patiënten gestart met chronische dialyse. Dit aantal is vergelijkbaar met voorgaande jaren. Het lijkt er wel op dat tijdens de eerste golf de start van chronische dialysebehandeling werd uitgesteld. Tijdens de eerste golf lag de instroom 11% lager ten opzichte van het gemiddelde van dezelfde periode gedurende de twee voorgaande jaren. De instroom per week van nieuwe patiënten met chronische dialyse jonger en ouder dan 65 jaar gedurende het jaar is weergegeven in figuur 2A en B. De lagere instroom is alleen zichtbaar bij oudere patiënten (>65 jaar); voor deze leeftijdscategorie was de daling 24%. In de tussenperiode lijkt sprake van een inhaaleffect bij ouderen. Ook in andere jaren is er sprake van aanzienlijke variatie en het is dan ook niet met zekerheid te zeggen dat dit patroon geheel te wijten is aan COVID-19.
Minder niertransplantaties
Door de COVID-19-pandemie zijn met name tijdens de eerste golf minder niertransplantaties uitgevoerd. In 2020 zijn 758 dialysepatiënten getransplanteerd, een afname van 13% ten opzichte van 2019. De totale effecten van COVID-19 op de transplantatiezorg worden uitgebreid beschreven in het vervolg van dit hoofdstuk.
Figuur 2. Incidentie dialyse (3-weeks voortschrijdend gemiddelde)
Hogere sterfte dialysepatiënten
In 2020 zijn 1.270 patiënten met chronische dialyse overleden. Dit komt overeen met 20% van de prevalente dialysepopulatie. Het aantal overlijdens was 15% hoger dan in 2019. De gemiddelde leeftijd van de overleden patiënten was 74,1 jaar. In 2018 en 2019 lag dit gemiddelde op 74,8 en 74,6 jaar respectievelijk.
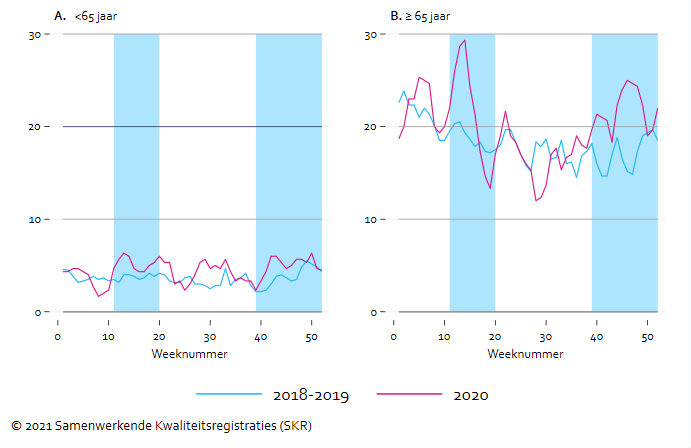
In absolute aantallen was de oversterfte het hoogste bij oudere patiënten (Figuur 3B). Met name aan het begin van de eerste golf was er sprake van een duidelijke piek, gevolgd door normale tot relatieve lage sterfte tijdens de tussenperiode. Ook tijdens de tweede golf was er aanzienlijke oversterfte in deze groep. Het aantal overlijdens in jonge patiënten (<65 jaar) was veel lager, maar relatief gezien is de oversterfte in 2020 in deze leeftijdscategorie juist hoger. Het aantal overlijdens onder patiënten jonger dan 65 jaar was 25% hoger dan het gemiddelde over 2018-2019. In oudere patiënten bedroeg de oversterfte 7%. Van 13% van de in 2020 overleden dialysepatiënten is bekend dat ze COVID-19 hebben gehad. De COVID-19-pandemie lijkt dus in belangrijke mate te hebben bijgedragen aan de geobserveerde oversterfte.
Figuur 3. Aantal overlijdens dialysepopulatie (3-weeks voortschrijdend gemiddelde)
COVID-19 in de dialysepopulatie
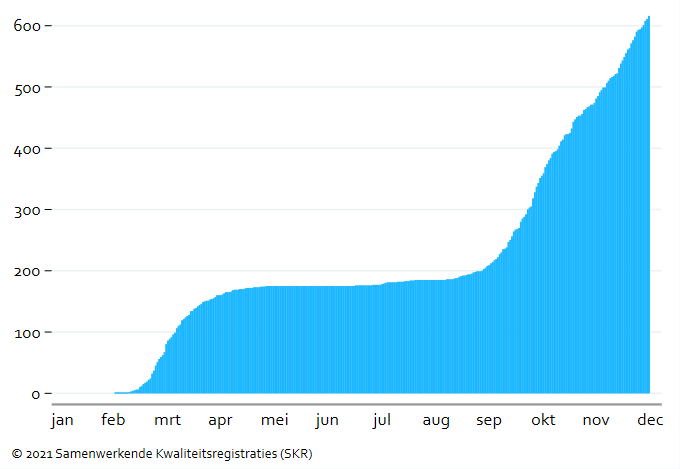
In 2020 zijn 616 dialysepatiënten met COVID-19 geregistreerd (Figuur 4). Dit komt overeen met bijna 10% van de dialysepopulatie. Tijdens de eerste golf was de incidentie hoog in vergelijking met de algemene bevolking. Dit is deels te verklaren doordat in dialysecentra frequenter getest wordt in het kader van isolatiemaatregelen. Incidentie in patiënten met thuisdialyse in de vorm van peritoneale dialyse lag dan ook beduidend lager. De hoogste incidentie, uitgedrukt naar grootte van de dialysepopulatie, was in de provincies Flevoland, Noord-Brabant en Zuid-Holland (Figuur 5).
Figuur 4. Cumulatief aantal dialysepatiënten met COVID-19 in 2020
Figuur 5. Regionale verdeling aandeel dialysepatiënten met COVID-19

Sterfte aan COVID-19
Ongeveer de helft van de dialysepatiënten met COVID-19 is opgenomen in het ziekenhuis, maar slechts een klein deel (4%) is op de IC terecht gekomen. Jonge dialysepatiënten zijn relatief vaker op de IC opgenomen. Ongeveer een kwart van de patiënten met COVID-19 is binnen 28 dagen na het vaststellen van COVID-19 overleden. Bij 22% van de patiënten is door het dialysecentrum aangegeven dat de patiënt is overleden ten gevolge van COVID-19. Leeftijd is hierbij een belangrijke risicofactor. Net als in de algemene bevolking hebben mannen een hoger risico dan vrouwen om aan de gevolgen van COVID-19 te overlijden.

TRANSPLANTATIE ZORG
Zoals beschreven in het hoofdstuk over acute zorg wordt de landelijke data over orgaan- en weefseltransplantatie verzameld door de Nederlandse Transplantatie Stichting (NTS). Deze fungeert tevens als orgaancentrum volgens de Wet op orgaandonatie inzake raadpleging donorregister, donoraanname, allocatie en transport van orgaan en weefsel.
Transplantatiezorg is acute en chronische zorg
Orgaantransplantatie is in het geval van een levende donor voor nier (of stukje van de lever) planbaar, maar in geval van een postmortale donor acuut. Daarom zijn de orgaantransplantaties met postmortale orgaandonoren ook kort beschreven in het hoofdstuk acute zorg.
In dit hoofdstuk wordt de transplantatiezorg iets meer uitgediept en maken we een onderscheid in a) nier- en pancreastransplantaties, b) lever-, hart- en longtransplantaties en c) weefseltransplantaties.
Transplantatiezorg bij nier- en pancreasfalen (niet acuut)
Nier- en pancreaspatiënten die op de wachtlijst staan voor een orgaantransplantatie kunnen een relatief langere wachttijd overbruggen in vergelijking met andere patiënten die wachten op een orgaantransplantatie; wel kan langer wachten hun kwaliteit van leven en medische conditie negatief beïnvloeden. Patiënten met eindstadium nierfalen hebben de mogelijkheid tot dialyse. Circa de helft van alle niertransplantaties wordt uitgevoerd met een levende-donornier; deze donatie is in tegenstelling tot de postmortale nierdonatie planbaar. Patiënten met een potentiële levende donor kunnen, met of zonder tijdelijke dialyse, in deze crisis de extra wachttijd overbruggen zonder grote kans op complicaties.
Pancreastransplantaties worden uitgevoerd bij patiënten met diabetes mellitus die niet goed instelbaar zijn met behulp van insuline; ook deze transplantatievorm heeft een minder acuut karakter.
Volume niertransplantaties sterk gedaald in eerste golf
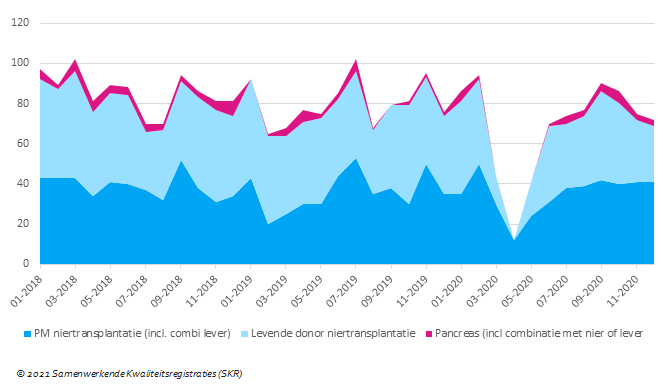
Mogelijkheid tot uitstel van de transplantatie voor de patiënt en het feit dat de donor ook kan wachten waren belangrijke argumenten om het programma nierdonatie bij leven tijdelijk te staken tijdens de eerste golf. Een andere belangrijke reden voor het tijdelijk staken van dit programma was dat de risico’s van een besmetting met het coronavirus bij zowel de levende donor als de ontvanger van de donornier onduidelijk waren. Daarnaast was tijdens de eerste golf nog niet bekend hoe patiënten met immunosuppressiva reageren op een COVID-19-besmetting. Normaal worden er gemiddeld 42 levende donor niertransplantaties per maand uitgevoerd (Figuur 6). Het staken van het programma nierdonatie bij leven heeft dus direct invloed gehad op veel patiënten.
De uitvoering van de niertransplantatieprogramma’s voor transplantaties met postmortale donornieren werd niet helemaal gestaakt. Een patiënt krijgt immers niet snel weer een nieuw aanbod van een passende nier; ook is het onwenselijk om een donornier verloren te laten gaan. Wel was er een daling van het aantal niertransplantaties vanwege het lagere aantal beschikbare postmortale donoren (zie hoofdstuk ‘Acute zorg’). Daarnaast was er een onderbreking van een aantal deelprogramma’s, zoals het transplanteren van nieren van oude (65+) donoren bij oudere patiënten. In 2018 en 2019 vonden er gemiddeld 38 postmortale donor niertransplantaties per maand plaats, maar in april 2020 slechts 12; een afname van 68%. In mei steeg het aantal weer en vanaf juli was het maandelijkse aantal transplantaties weer op normaal niveau. Meer informatie over de eerste golf is terug te vinden in de publicatie uit 2020 vanuit de Nederlandse Transplantatie Vereniging en de Nederlandse Transplantatie Stichting.4
Figuur 6. Levende en postmortale donor niertransplantaties en pancreastransplantaties van 2018 t/m 2020 (cumulatief, inclusief combinaties met andere organen)
Geen stopzetting nierprogramma’s in tweede golf
Tijdens de tweede golf werd het niertransplantatieprogramma normaal gecontinueerd omdat de risico’s van COVID-19 bij chronische dialyse hoger worden ingeschat dan na niertransplantatie.5 Vanaf november 2020 zagen we een daling van het aantal levende-donor niertransplantaties tot gemiddeld 30 per maand. Iets later, in februari en maart 2021 daalde ook het aantal postmortale niertransplantaties weer naar gemiddeld 30.
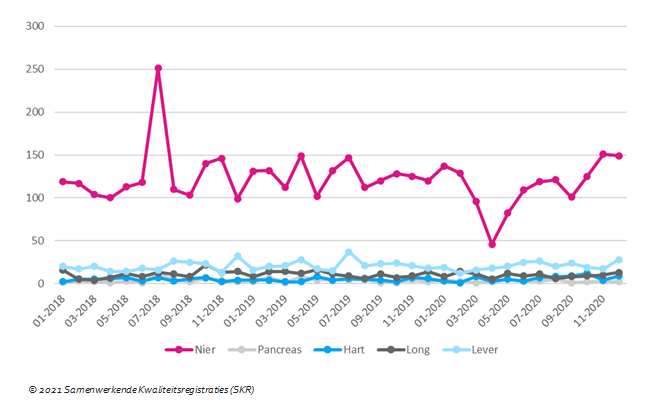
Naast een daling van het aantal transplantaties is er in de eerste golf ook een daling van de instroom op de nierwachtlijst te zien (Figuur 7). Vanwege verwachte lagere transplantatiekansen tijdens de eerste golf en vanwege een lager aantal verwijzingen naar de transplantatiecentra zijn minder patiënten op de nierwachtlijst geplaatst. Na de eerste golf veerde de instroom terug, maar een echte inhaalslag was niet te zien in de rest van 2020, vanwege druk op de transplantatiepoliklinieken. De instroompiek in juli 2018 werd veroorzaakt door het inhalen van achterstallige inschrijvingen van één centrum. Dit geeft aan dat het eventuele inhalen van inschrijvingen wel direct zichtbaar zou moeten zijn.
Het aantal transplantabele patiënten op de wachtlijst voor een postmortale donornier is de actieve nierwachtlijst. De actieve nierwachtlijst is in 2020 niet substantieel gegroeid, dankzij de snelle hervatting van niertransplantatie en de afwezigheid van de inhaalslag van de inschrijvingen op de wachtlijst (data niet getoond).
Pancreastransplantaties alleen tijdens eerste golf gestaakt
Tijdens de eerste golf zijn de pancreastransplantatieprogramma’s gestaakt (Figuur 6). De redenen hiervoor zijn dat de patiënten de mogelijkheid hebben om te wachten; daarnaast waren de effecten van een COVID-19-besmetting in combinatie met de immunosuppressiva na transplantatie nog niet duidelijk. Normaal gesproken vinden er gemiddeld drie pancreastransplantaties per maand plaats. De programma’s zijn in juni weer gestart en tijdens de tweede golf gecontinueerd. De pancreaswachtlijst-instroom bleef gelijk tijdens de eerste golf (Figuur 7). Door het staken van het pancreastransplantatieprogramma was de pancreaswachtlijst langer na de eerste golf. Tegen het einde van het jaar was deze weer terug op het niveau van begin 2020.
Figuur 7. Instroom van patiënten op de orgaantransplantatiewachtlijsten in 2018 t/m 2020 per maand en per orgaan
Daling volumina andere transplantaties
Volume hart, lever en longtransplantaties licht gedaald in eerste golf
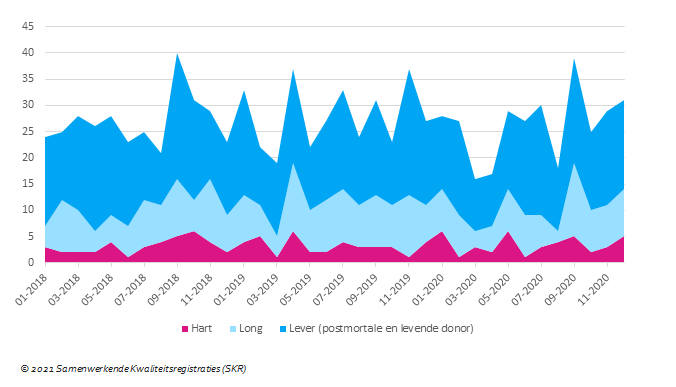
In aanvulling op het hoofdstuk over de acute zorg laten we in figuur 8 zien dat de daling van het aantal hart-, long- en levertransplantaties gezamenlijk minder sterk was in vergelijking met de nier- en pancreastransplantaties. Dit heeft te maken met het urgente karakter van dit type transplantaties en de afwezigheid van goede alternatieve behandelvormen. Levertransplantatie daalt in absolute zin het meeste, gevolgd door longtransplantatie. Bij harttransplantatie zijn de aantallen per maand laag en lijkt er geen duidelijke dip te zijn geweest in de eerste golf. Deze transplantaties zijn urgenter omdat er geen goed alternatief is voor transplantatie; deze transplantaties zijn dus niet gestaakt, maar waren wel afhankelijk van het postmortale donoraanbod en de benodigde IC-capaciteit voor zowel de donorprocedure als de postoperatieve IC-opname van de ontvanger. Na de eerste golf konden deze transplantatieprogramma’s weer normaal worden uitgevoerd. Tijdens de tweede golf was er voldoende capaciteit en waren er voldoende orgaandonoren voor deze transplantatieprogramma’s om normaal door te gaan. Een klein deel van de levertransplantaties wordt uitgevoerd met een stuk lever van levende donoren (gemiddeld twee per maand). Dit werd net als het programma nierdonatie bij leven gestaakt tijdens de eerste golf. Tijdens de tweede golf was het aantal levende donor levertransplantatie met gemiddeld drie transplantaties per maand iets hoger dan normaal.
De lever- en longwachtlijst zijn gelijk gebleven, maar de hartwachtlijst is aan het eind van 2020 toegenomen (www.transplantatiestichting.nl). Tijdens de eerste golf is een deel van de leverpatiënten op acute wachtlijst op een niet-transplantabele urgentie geplaatst. Dit werd gedaan om ervoor te zorgen dat bij het verminderde aanbod van donorlevers de patiënten met de kortste overlevingskans op de leverwachtlijst als eerste werden getransplanteerd.
Figuur 8. Hart-, long- en levertransplantaties (cumulatief, inclusief levende donor lever transplantaties en combinaties met andere organen) in 2018 t/m 2020 per maand en per orgaan
Volume weefseltransplantaties alleen sterk gedaald in eerste golf
In figuur 9 is te zien dat het volume voor weefseldonaties tijdens de eerste golf sterk daalt, maar daarna weer wordt hervat. De gedoneerde weefsels zijn hoornvlies, hartklep, huid en bot. De hoornvliestransplantaties laten eenzelfde trend zien als de donaties. Na de eerste golf is deze vorm van transplantatie ook hervat en tijdens de tweede golf zien we geen significante daling.
Figuur 9. Aantal postmortale weefseldonoren in 2019 en 2020 per maand (incl. lijn van gemiddelde over 2018-2019)
BESCHOUWING
Doordat de diabetesregistratie (DPARD) nog geen landelijke dekking heeft, is het niet mogelijk een goede inschatting te geven van de impact van de COVID-19-pandemie op de tweede en derdelijns-diabeteszorg. In een vijftal ziekenhuizen werden echter wel aanzienlijk minder patiënten op de polikliniek gezien dan in het voorgaande jaar.
De chronische dialysezorg is zo goed als mogelijk normaal voortgezet. Wel lijkt het erop dat bij oudere patiënten tijdens de eerste golf de start van dialysebehandeling is uitgesteld. Deze achterstand is later weer ingehaald. Een belangrijk gevolg van de COVID-19-pandemie is dat in 2020 minder dialysepatiënten, een daling van 13%, een donornier hebben ontvangen met mogelijk negatieve gevolgen voor hun gezondheid. Een transplantatie zorgt voor een betere overleving en ook voor een betere kwaliteit van leven.
Naast indirecte gevolgen van COVID-19 door uitgestelde zorg is er binnen de dialysepopulatie met name een groot direct effect zichtbaar. In 2020 heeft ongeveer 10% van de dialysepatiënten COVID-19 gehad, met een aanzienlijke oversterfte tot gevolg. Het aantal overlijdens was 15% hoger dan in 2019. Dialysepatiënten zijn kwetsbaar en deze populatie heeft daarom prioriteit gekregen binnen het vaccinatieprogramma.
De impact van COVID-19 was het meest evident voor de transplantatiezorg. Tijdens de eerste golf zijn het levende-donornier programma en de programma’s voor pancreastransplantaties zelfs geheel stopgezet. Redenen waren de beperkte IC-capaciteit, maar ook de ingeschatte risico’s van een COVID-19-besmetting in combinatie met immunosuppressiva waarmee transplantatiepatiënten worden behandeld. Tijdens de eerste golf is er veel kennis opgedaan waardoor tijdens de tweede golf de verschillende transplantatieprogramma’s zo goed als mogelijk konden doorgaan. Daarnaast is er veel energie gestoken in goede infrastructuur, communicatie en landelijke afspraken tussen ziekenhuizen, het RIVM en de Nederlandse Vereniging voor Intensive Care om donatie en transplantatie mogelijk te maken. De achterstanden zijn gedurende het jaar echter niet ingelopen.
Het lijkt aannemelijk dat patiënten met chronische aandoeningen, met name tijdens de eerste golf, het ziekenhuis hebben gemeden of dat zorg is uitgesteld door de zorgverleners. In hoeverre deze zorg later is ingelopen is nog niet duidelijk. Uitstel van zorg heeft mogelijk geleid tot verslechtering van de gezondheidstoestand, die pas later meetbaar wordt. Monitoring door middel van langdurige registraties is dan ook belangrijk. Veel patiënten hebben verschillende aandoeningen en alleen door de diverse registraties goed op elkaar aan te laten sluiten, kan een compleet beeld worden verkregen.
De COVID-19-pandemie heeft gezorgd voor versnelde digitalisering in de zorg. Zorg op afstand kan in de toekomst helpen voorkomen dat een deel van de patiënten uit zicht raakt. Daarmee kan zorg op afstand een belangrijke rol spelen in het minimaliseren van negatieve gevolgen van een pandemie op reguliere zorg voor chronische patiënten.
Referenties
- BIDON. Diabetes-Toetsingskader Kwaliteitsregistraties. 2017.
- Webster AC, Nagler E V., Morton RL, Masson P. Chronic Kidney Disease [Internet]. Vol. 389, The Lancet. Lancet Publishing Group; 2017 [cited 2021 Apr 28]. p. 1238–52. Available from: http://www.thelancet.com.vu-nl.idm.oclc.org/article/S0140673616320645/fulltext
- Bardenheier BH, Lin J, Zhuo X, Ali MK, Thompson TJ, Cheng YJ, et al. Disability-free life-years lost among adults aged ≥50 years with and without diabetes. Diabetes Care [Internet]. 2016 Jul 1 [cited 2020 Oct 12];39(7):1222–9. Available from: https://pubmed.ncbi.nlm.nih.gov/26721810/
- A.P.J. de Vries et al. Immediate impact of COVID-19 on transplant activity in the Netherlands. Transpl Immunol. 2020; 61: 101304.
- L.B. Hilbrands et al. COVID-19-related mortality in kidney transplant and dialysis patients: results of the ERACODA collaboration. Nephrol Dial Transplant. 2020; 35: 1973–1983.
Welke registraties hebben aan dit hoofdstuk bijgedragen?
Diabetesregistratie (DPARD)
In 2017 heeft stichting BIDON, een landelijk consortium van internisten, kinderartsen en diabetespatiënten, kwaliteitsregistratie DPARD (Dutch Pediatric and Adult Registry of Diabetes) voor diabetes mellitus in de tweede en derde lijn gelanceerd. DPARD omvat zowel kinderen als volwassenen. Data wordt niet handmatig geregistreerd maar verzameld vanuit het elektronische patiënten dossier (EPD). Gegevens dienen hiervoor discreet (op de juiste plaats en op de juiste manier) in het EPD te worden vastgelegd. Data aanlevering voor DPARD wordt op dit moment per patiënt minimaal eenmaal per jaar gedaan. Als bepaalde onderzoeken of verrichtingen meermaals per jaar plaatsvinden wordt uitgegaan van de laatst uitgevoerde verrichting of onderzoek.
Dialyseregistratie (Renine)
Renine (Registratie Nierfunctievervanging Nederland) is de registratie van alle patiënten in Nederland met een nierfunctievervangende behandeling. Patiënten worden gevolgd vanaf start dialyse of niertransplantatie tot overlijden. Gegevens van dialysepatiënten worden aangeleverd door alle Nederlandse dialysecentra. De transplantatiegegevens in Renine zijn afkomstig uit de Nederlandse Orgaantransplantatie Registratie (NOTR) van de Nederlandse Transplantatiestichting (NTS). Renine bestaat sinds 1986 en wordt beheerd door de stichting Nefrovisie in Utrecht. Nefrovisie is het landelijk kwaliteitsbureau voor de behandeling van nierziekten.
Transplantatie registratie (NTS)
De Nederlandse Transplantatie Stichting is volgens de Wet op de orgaandonatie verantwoordelijk voor het proces van donatie, allocatie, transplantatie en wachtlijst voor organen (nier, lever, hart, long, pancreas) en weefsels (oogweefsel, huid, bot, hartkleppen, lichaamsaders) in Nederland. De NTS legt data hierover vast. Tevens beheert de NTS de kwaliteitsregistratie NOTR waarin de follow-up van transplantatiepatiënten en levende donoren wordt verzameld ten behoeve van beleidsevaluatie en wetenschappelijk onderzoek.
In de analyse van het acute cluster van dit rapport wordt het totaal aan postmortale orgaandonaties en transplantaties getoond. In dit hoofdstuk worden de levende donaties evenals de postmortale orgaantransplantaties getoond, gedifferentieerd naar orgaan.
